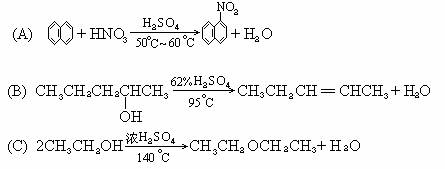
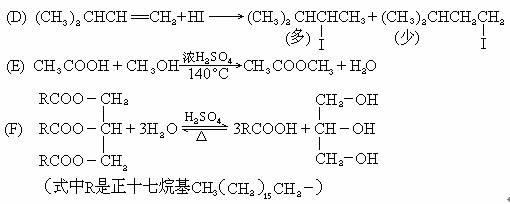
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可作有机溶剂.
实验室中制备硝基苯的过程如下:
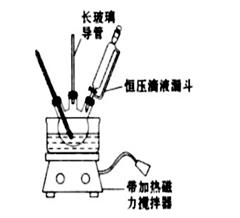 ①配制混酸:组装如图反应装置.取100ml烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,加入恒压滴液漏斗中.把18mL苯加入三颈烧瓶中.
①配制混酸:组装如图反应装置.取100ml烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,加入恒压滴液漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀.
③加热在50~60℃下发生反应,直至反说结束.
④除去混合酸后,粗产品依次用蒸馏水和10%Na2CO3溶液
洗涤,最后用蒸馏水洗涤得到粗产品.
⑤为了得到更纯净的硝基苯.还需先向液棒中加人试剂A,
静置一段时间后弃去试剂A,然后蒸馏,最终得到17.5g
硝基苯
已知(1)
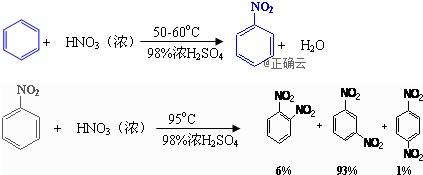
可能用到的有关数据列表如下:
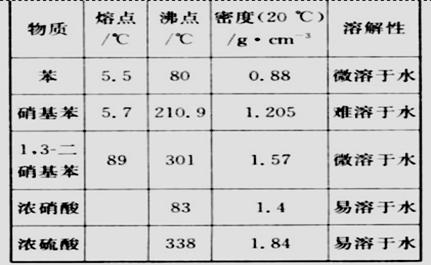
请回答下列问题:
(1)配制混酸应先在烧杯中加入___ __.
(2)恒压滴液漏斗的优点是___ ___,
实验装置中长玻璃导管可用______ 代替(填仪器名称)
(3)要控制反应温度50~60℃,可用水浴加热,其优点为____ __
(4)反应结束后产品在液体的_____层(填"上"或"下"),分离混酸和产品的操作方法为__ ___
(5)用10% Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?___
__
(6)试剂A是___ __,蒸馏过程中需在蒸馏烧瓶中加入沸石,其作用为___ __
若加热后,发现未加沸石,应采取的正确方法___ __
(7)硝基苯的产率为__ ___.
答案
(1)浓硝酸 (1分)
(2)可以保持一斗内压强与发生器内压强相等,使漏斗内液体顺利流下冷凝管(球形冷凝管或直形冷凝管均可)(1分)
(3)受热均匀,温度容易控制(1分)
(4)上 (1分) 分液(1分)
(5)取最后一次洗涤液,加入氯化钙溶液,无沉淀生成,说明已洗净(2分)
(6)氯化钙, (1分) 防止暴沸, (1分) 停止加热,冷却后补加, (1分)
(7)70% (2分)

 )与两个烃基相连的化合物叫做酮。饱和一元酮的通式为
)与两个烃基相连的化合物叫做酮。饱和一元酮的通式为