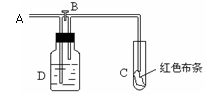
下图是某化学兴趣小组在实验室用二氧化锰和浓盐酸制取干燥纯净的氯气并进行相关性质实验的装置,请你回答下列问题:
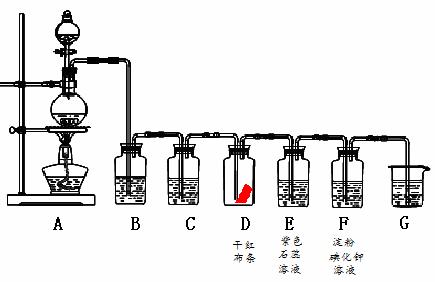 |
(1) 装置A中发生反应的化学方程式: ,
(2) B中的试剂是 ,作用是 ,
(3) C中的试剂是 ,作用是 ,
(4) D中的干红布条 (褪色、不褪色)
(5) E中的现象是 ,
(6) F中的现象是 、反应方程式 ,
(7) G中的试剂是 、反应方程式 ,
(8) 用含有0.4molHCl的浓盐酸与足量的MnO2充分反应,收集产生的全部氯气在标准状况下的体积总是小于2.24L,分析其原因: 。
答案
(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)饱和食盐水、除去氯气中的氯化氢气体
(3)浓硫酸、干燥氯气
(4)不褪色
(5)溶液先变红后褪色
(6)溶液变蓝、Cl2 + 2KI = 2KCl + I2
(7)NaOH溶液、2NaOH + Cl2 = NaCl + NaClO + H2O
(8)氯化氢挥发、随着反应的进行,盐酸浓度减小,稀盐酸与二氧化锰不反应。




 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。  2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。  HCl+HClO
HCl+HClO