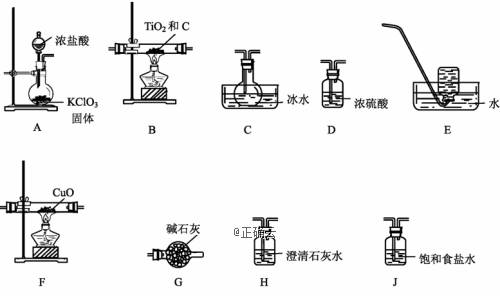
钛(Ti)被誉为第三金属,广泛应用于航空航天等领域。四氯化钛(TiCl4)是生产金属钛的重要原料,某小组设计实验制备四氯化钛并验证其产物CO,装置如下:
已知部分信息如下:
①制TiCl4的反应原理为:TiO2(S)+2C(s)+2Cl2(g) ![]() TiCl4(g)+2CO(g) ②四氯化钛的熔、沸点分别为-24℃、136℃,易挥发,在水或淛湿空气中都极易水解,加热时能被O2氧化
TiCl4(g)+2CO(g) ②四氯化钛的熔、沸点分别为-24℃、136℃,易挥发,在水或淛湿空气中都极易水解,加热时能被O2氧化
回答下列问题:
(1)气流由左至右,装置的正确连接顺序为:A、______________________、H、E(填字母)。
(2)A中盛装盐酸的仪器名称是___________;G装置的作用是______________________。
(3)写出A中发生反应的化学方程式:______________________;实验室欲制备6720mLCl2(标准状态),则理论上应转移___________mol电子。
(4)能证明上述反应有CO生成的实验现象是______________________。
(5)利用右图所示装置测定产品纯度:取 w g TiCl4产品进行实验,向安全漏斗中加入适量蒸馏水,待四氯化钛充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴
0.1mol·L-1;的K2CrO4溶液作指示剂注明:Ag2CrO4呈砖红色),用cmol·L-1AgNO3溶液滴定至终点,消耗滴定液VmL。【已知:常温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12。TiCl4+(2+n)H2O=TiO2·nH2O↓+4HCl】
①安全漏斗在本实验中的作用除加水外,还有______________________。
②根据上述数据计算该产品的纯度为___________(用含w、c和V的代数式表示)。
答案


 。
。 C+MgO
C+MgO  MgO+H2O
MgO+H2O  2MgO
2MgO MgCl2
MgCl2  MgS
MgS Mg3N2
Mg3N2  Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq) Mg+Cl2↑
Mg+Cl2↑