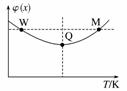
在2 L恒容密闭容器中充入2 mol X和1 mol Y,发生反应:2X(g)+Y(g)3Z(g) ΔH<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
A.升高温度,平衡常数增大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
答案
解析:A项,分析图像,X的体积分数先减小后增大,减小到最低,这是化学平衡的建立过程,后增大,这是平衡的移动过程,升高温度,体积分数增大,说明升高温度,平衡向左移动,使平衡常数减小,故A错;B项,M点温度高,故反应速率快,B错误;从开始到Q点是正向建立平衡的过程,转化率逐渐增大,从Q到M点升高温度,平衡向左移动,使转化率降低,Q点最大,故C正确;平衡时再充入Z,达到的新平衡与原平衡是等效的,故体积分数相等,D错。
答案:C
