电化学在生产生活中有广泛的应用。
(1)高铁电池因其储电容量大而开始应用于电动汽车。已知该电池放电时的总反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2,则电解质溶液可能为________(填字母)。
A.KOH 溶液 B.H2SO4 C.稀HNO3
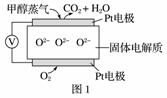
(2)甲醇燃料电池能大幅度地提高甲醇的利用率,其工作原理如图1所示,电解质是掺杂了Y2O3的ZrO2晶体,它能传导O2-。工作时O2-向________(填“正极”或“负极”)移动,负极的电极反应式为________________。
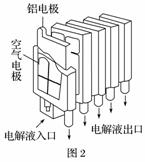
(3)铝-空气电池装置如图2所示,该电池的负极是________(填“铝电极”或“空气电极”),毎消耗0.54 g Al,需消耗标准状况下的空气______L(设空气中O2的体积分数为20%)。
答案
答案 (1)A (2)负极 CH3OH+3O2--6e-===CO2+2H2O (3)铝电极 1.68
解析 (1)根据电池放电时的总反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2,生成物Fe2O3、ZnO能够被酸溶解,电解质溶液应该选KOH 溶液。
(2)甲醇燃料电池中充入甲醇的电极是负极,通入氧气的电极是正极,工作时O2-向负极移动,负极上甲醇发生氧化反应,电极反应式为CH3OH+3O2--6e-===CO2+2H2O。
(3)铝-空气电池的负极是铝电极,空气电极是正极;0.54 g Al的物质的量为![]() =0.02 mol,反应后转移电子0.06 mol,需要氧气的物质的量为
=0.02 mol,反应后转移电子0.06 mol,需要氧气的物质的量为![]() =0.015 mol,需消耗标准状况下的空气的体积为0.015 mol×22.4 L·mol-1÷20%=1.68 L。
=0.015 mol,需消耗标准状况下的空气的体积为0.015 mol×22.4 L·mol-1÷20%=1.68 L。
