为了缓解温空效应,科学家提出了多种回收和利用CO2的方案。
(1) 方案1: 利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 = + 113. 4kJ/mol
则 3FeO(g)+H2O(g)= Fe3O4(s)+H2(g) ΔH3 = 。
方案2:利用CO2制备CH4
 300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应:CO2(g)+4H2(g)
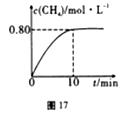
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应:CO2(g)+4H2(g)![]() CH4(g)+ 2H2O(g)ΔH4,混合气体中CH4的浓度与反应时间的关系如图17所示。
CH4(g)+ 2H2O(g)ΔH4,混合气体中CH4的浓度与反应时间的关系如图17所示。
(2)①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)= 。
②300℃时,反应的平衡常数K= 。
③保持温度不变,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度 (填序号)。
A.等于0.8mo/L B.等于1.6mo/L C.0.8mol/L<c(CH4)<1.6mol/L D.大于1.6mol/L
(3)300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g).则v正 v逆
(填“>”“<”或“=" )。
(4)已知:200℃时,该反应的平衡常数K=64.8L2·mol-2。则ΔH4 0(填“>”“<”或“=”)。
 方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图18所示:(假设开始时两极的质量相等)
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图18所示:(假设开始时两极的质量相等)
(5)①放电时,正极的电极反应式为 。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mole-时,两极的质量差为 g。
(6)室温下,物质的量浓度均为0.lmol/L 的几种含碳盐溶液的pH如下表:
| 序号 | ① | ② | ③ |
| 溶液 | NaHCO3 | NaX | Na2CO3 |
| pH | 8.4 | 9.7 | 11.6 |
写出溶液②中通入少量CO2的离子方程式: .
等体积的①和③形成的混合溶液中离子浓度由大到小排列为: .
答案
【答案】(共15分)(1)+18.7kJ/mol (2分)
(2)①0.32mol·L−1·min−1 (1分) ②25 L2·mol−2 (1分) ③D (1分)
(3)> (1分)
(4)< (1分)
(5)①3CO2+4Na++4e−=2Na2CO3+C (2分) ②15.8 (2分)
(6)X−+CO2+H2O=HCO![]() +HX(2分) c(Na+)>c(HCO3-)>c(CO32-)> c(OH-)> c(H+)(2分)
+HX(2分) c(Na+)>c(HCO3-)>c(CO32-)> c(OH-)> c(H+)(2分)
