三氯氧磷(POCl3)是一种工业化工原料。无色透明的带刺激性臭味的液体,在潮湿空气中剧烈发烟。某化学小组采用PCl3氧化法制备POCl3。已知: POCl3的熔点为-112℃,沸点为75.5℃。在潮湿空气中二者均极易水解面剧烈“发烟”。回答下列问题:
I.制备PCl3
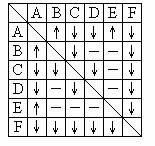
(1)实验室用高锰酸钾和浓盐酸反应制取氯气。发生装置可以选择图中的_____(填字母代号)。
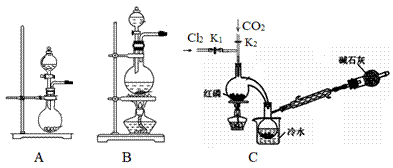
(2)检查装置气密性并装入药品后,先关闭K1,打开K2通入干燥的CO2,一段时间后, 关闭K2,加热曲颈瓶同时打开K1通入干燥氯气,反应立即进行。通干燥CO2的作用是_______。
II.制备POCl3(如图)
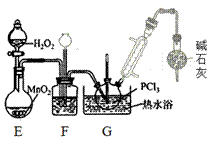
(3)盛放碱石灰的仪器的作用是________,装置G中发生反应的化学方程式为________ 。
(4) 装置F的作用除观察O2的流速之外,还有________。
III.测定POCl3含量
实验制得的POCl3中常含有PCl3杂质,通过下面方法可测定产品的纯度:
①快速称取5.000g产品,加水反应后配成250mL溶液;
②取以上溶液25. 00mL,向其中加入10. 00mL 0.1000mol/L碘水(足量),充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3溶液滴定;
④重复②、③操作,平均消耗0.1000mol/LNa2S2O3溶液8.00mL.
已知: H3PO3+I2+H2O==H3PO4+2HI,I2+2Na2S2O3==2NaI+Na2S4O6.
(5)滴定终点的现象为__________。该产品的纯度为________。
(6)若滴定管在滴定前无气泡,滴定后有气泡,则测定结果______(填“偏高”“偏低” 或“不变”)。
答案
【答案】 (1). A (2). 防止红磷被氧气氧化和生成的 PCl3与空气中的 O2和水反应 (3). 隔离空气中的水蒸气,防止水解 (4). 2PCl3+O2=2POCl3 (5). 平衡气压、干燥氧气 (6). 当最后一滴标准液滴入时,溶液由蓝色变为无色,且半分钟内不变色 (7). 83.5% (8). 偏低
【解析】分析:本题是一道和制备相关的实验题,涉及实验装置的选择;实验操作的分析;仪器中药品的作用;装置的作用;纯度计算;误差分析。
详解:I.(1)实验室用高锰酸钾和浓盐酸反应制备氯气,发生:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,反应不需要加热,故选A;
(2)由于红磷易被氧化和PCl3易被氧化和水解,反应前通干燥CO2排除装置中的空气,防止红磷被氧气氧化和生成的 PCl3与空气中的 O2和水反应,本题答案为:防止红磷被氧气氧化和生成的 PCl3与空气中的 O2和水反应。
II. (3) 为防止外界水蒸气进入G使PCl3水解,干燥管中盛放碱石灰,装置G中发生PCl3被氧化成POCl3的反应,化学方程式为2PCl3+O2=2POCl3 ;本题答案为:隔离空气中的水蒸气,防止水解;2PCl3+O2=2POCl3 。
(4) 装置F中的长颈漏斗,可以平衡压强,起到安全瓶的作用,所以装置F的作用除观察O2的流速之外,还有平衡气压、干燥氧气;本题答案为:平衡气压、干燥氧气。
III. (5)依据反应原理,滴定终点的现象为当最后一滴标准液滴入时,溶液由蓝色变为无色,且半分钟内不变色;
关系式:PCl3![]() H3PO3
H3PO3 ![]() I2,I2
I2,I2![]() 2Na2S2O3;
2Na2S2O3;
消耗Na2S2O3的物质的量=0.1000mol/L×8.00×10-3L=8×10-4mol,
和Na2S2O3反应的I2的物质的量=![]() ×8×10-4mol=4×10-4mol,
×8×10-4mol=4×10-4mol,
PCl3的物质的量=和PCl3反应的I2的物质的量=0.1000mol/L×10.00×10-3L-4×10-4mol=6×10-4mol,
PCl3的质量=6×10-4mol×137.5g/mol=8.25×10-2g,
样品中含PCl3的质量=8.25×10-2g×![]() =0.825g,样品纯度=
=0.825g,样品纯度=![]() ×100%=83.5%;
×100%=83.5%;
(6)若滴定管在滴定前无气泡,滴定后有气泡,则消耗Na2S2O3溶液的体积偏小,导致计算出的PCl3的质量偏大,测定结果则偏低。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L