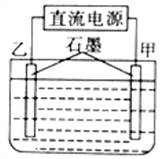
用图所示装置电解硫酸铜和氯化钠的混合溶液,当线路中有1.20mol电子通过时,甲电极增重并有4.48L (已折算成标准状况下的体积,后同)气体生成,乙电极同时生成气体7.84L,则原溶液中硫酸铜与氯化钠的物质的量之比为
A. 2:1 B. 4:1 C. 2:3 D. 4:3
答案
【答案】A
【解析】分析:本题考查电解原理,根据离子放电顺序,分析电极产物,根据电子守恒解答。
详解:该电解池可能发生的阴极反应为:①Cu2++2e-=Cu、②2H++2e-=H2↑;发生的阳极反应为:③2Cl--2e-=Cl2↑,④2H2O-4e-=4H++O2↑,甲电极增重,并有4.48L气体生成,则氢气体积为4.48L(标准状况),乙电极同时生成气体7.84L(氯气和氧气),反应共转移电子1.20mol,阴极反应中,反应②共得电子0.4mol电子,则反应①共得电子1.2mol-0.4mol=0.8mol,可计算得原溶液中含Cu2+,其物质的量为0.4mol;设阳极产生氯气物质的量为x,产生氧气物质的量为y,则x+y=![]() =0.35mol,共转移电子1.2mol,则2x+4y=1.2,联立两个方程,解得,x=0.1mol,y=0.25mol,所以溶液中含Cl-为0.2mol, 则原溶液中硫酸铜与氯化钠的物质的量之比为0.4:0.2=2:1,故选A项。综上所述,本题正确答案为A。
=0.35mol,共转移电子1.2mol,则2x+4y=1.2,联立两个方程,解得,x=0.1mol,y=0.25mol,所以溶液中含Cl-为0.2mol, 则原溶液中硫酸铜与氯化钠的物质的量之比为0.4:0.2=2:1,故选A项。综上所述,本题正确答案为A。
