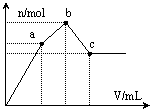
某化学小组欲进行如下实验探究金属与浓硫酸反应。试回答下列问题。
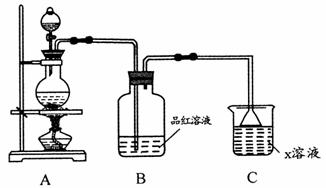
(1)利用上图装置研究铜与浓硫酸反应,反应化学方程式为_________; B装置的目的是______; x溶液为___________。
(2)将上述实验中的铜改为黄铜(铜锌合金),实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快。该气体可能为____,气体产生越来越快的原因可能是_____(答一点即可)。
验证该气体的实验方案如下:
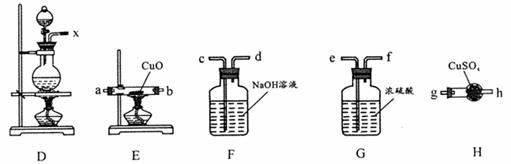
①装置连接顺序:x→_________;
②能证明上述假设成立的实验现象是__________。
答案
(1)Cu+ 2H2SO4(浓)![]() CuSO4+SO2↑+ 2H2O(2分);检验产物SO2(2 分);NaOH溶液(其他合理答案均可得分)(2分)
CuSO4+SO2↑+ 2H2O(2分);检验产物SO2(2 分);NaOH溶液(其他合理答案均可得分)(2分)
(2)H2(2分) ;反应后期,c(H+)增大,与Zn反应生成H2 速率加快;黄铜为铜锌合金,与硫酸形成原电池产生H2 速率加快;反应放热(2 分,其它合理答案也可给分)
①c→d→e→f→a→b→g (2分,不全对不得分)
②E中(硬质玻璃管)黑色粉末变红,H中(球形干燥管)固体由白色变为蓝色(2 分,不全扣1分,其它合理也给分)

 (纯氧中发出耀眼的白光)
(纯氧中发出耀眼的白光) (Al2S3在溶液中完全双水解)
(Al2S3在溶液中完全双水解)
 (AlN与水反应生成Al(OH)3和NH3↑)
(AlN与水反应生成Al(OH)3和NH3↑) 




 ,
, ,所以根据得失电子守恒可知:
,所以根据得失电子守恒可知: ,利用此关系可以方便地进行有关计算。
,利用此关系可以方便地进行有关计算。