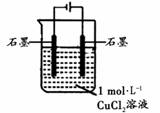
某小组同学利用下图装置对电解氯化铜实验进行了研究。
| 装置 | 现象 |
|
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的 是溶液变绿的原因。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl_![]() [CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因: 。
[CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因: 。
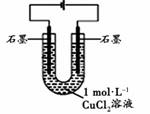
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
| 装置 | 现象 |
|
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U型管变热,冷却后阴极附近溶液仍为绿色 |
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是 ,否定乙的依据是 。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]_,[CuCl2]_掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]_的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]_掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]_的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是 。
② 写出b中生成[CuCl2]_的离子方程式: 。
③ 补充c中必要的操作及现象: 。
丙据此得出结论:电解时阴极附近生成[CuCl2]_是导致溶液变绿的原因。
答案
(14分)(1)Cl2
(2)电解过程放热导致温度升高,Cu2+ + 4Cl-![]() [CuCl4]2-正向移动;
[CuCl4]2-正向移动;
(3)阳极附近溶液仍为蓝色;U型管冷却后阴极附近溶液仍为绿色;
(4)①证明在上述实验条件下,电解后的绿色溶液中存在[CuCl2]-;
②Cu2+ + 4Cl-+ Cu = 2[CuCl2]-;
③加入CuCl2蓝色溶液,直至溶液颜色与电解后绿色溶液基本相同。