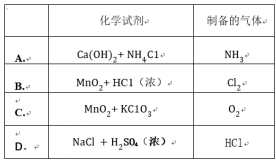
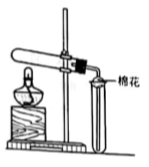
(1)连接好装置后,先___________。
(2)向烧瓶里加入少量___________粉末,分液漏斗中注入密度为1.19 g·cm-3的___________,慢慢地将分液漏斗中的液体注入烧瓶。
(3)___________加热,氯气便能放出。
(4)A中盛放的是___________,其作用为__________________________________。
(5)B中盛放的是___________,其作用为__________________________________。
(6)C的要求和作用是_______________________________________________。
(7)D中盛放的是___________,其作用为_________________________________。
(8)从中可以得出氯气的物理性质为__________________________________________。
答案
解析:由制Cl2的反应特点确定气体发生装置,有杂质HCl、H2O的存在考虑A、B净化装置,Cl2能溶,比空气重,确定了用长进短出排气法收集,而Cl2有毒应进行尾气处理。
答案:(1)检查气密性 (2)MnO2 浓盐酸 (3)酒精灯 (4)饱和NaCl 吸收HCl (5)浓H2SO4 除H2O (6)长进短出,收集Cl2 (7)NaOH溶液 吸收多余Cl2 (8)黄绿色气体,不溶于饱和NaCl溶液