研究NOx、CO等大气污染气体的处理及利用的方法具有重要意义,可实现绿色环保、节能
减排、废物利用等目的。
(1) 利用甲烷催化还原NOx:
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160 kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为
(2) 已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反
应: CO(g)+H2O(g)![]() H2(g)+CO2(g),500 ℃时的平衡常数为9,若在该温度下进行反应,设
H2(g)+CO2(g),500 ℃时的平衡常数为9,若在该温度下进行反应,设
起始时CO和H2O的浓度均为0.02 mol·L-1,则CO的平衡转化率为 。
(3) 用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图1所示。


图1 氨气选择性还原NO反应历程 图2 气体中含氮组分浓度随温度变化
①写出总反应的化学方程式: 。
②测得该反应的平衡常数与温度的关系为lg K=5.08+,该反应是 (填“吸热”或
“放热”)反应。
③该反应的含氮气体组分随温度变化如图2所示,当温度达到700 K时,发生副反应的化学
方程式为 。
(4) 图3是用食盐水作电解液电解烟气脱氮的一种原理图,NO被阳极产生的氧化性物质氧化为N,尾气经氢氧化钠溶液吸收后排入空气。图4是电流密度和溶液pH对烟气脱硝的影响。
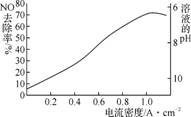
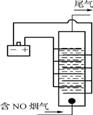
图3 图4 电流密度、pH对NO去除率的影响
①NO被阳极产生的氧化性物质氧化为N反应的离子方程式为
。
②溶液的pH对NO去除率影响的原是 。
③若极板面积为10 cm2,实验烟气含NO 1.5%,流速为0.070 L·s-1(气体体积已折算成标准状况,
且烟气中无其他气体被氧化),法拉第常数为96 500 C·mol-1,测得电流密度为1.0 A·cm-2。
列式计算实验中NO去除率: 。
答案
(1) CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ· mol-1
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ· mol-1
(2) 75%
(3) ①4NH3+4NO+O2![]() 4N2+6H2O ②放热 ③4NH3+5O2
4N2+6H2O ②放热 ③4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
(4) ①3Cl2+8OH-+2NO![]() 2N+6Cl-+4H2O ②次氯酸钠在酸性条件下氧化性增强
2N+6Cl-+4H2O ②次氯酸钠在酸性条件下氧化性增强
③×100%=73.7%
