氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,只有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
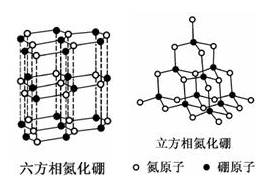
(1)基态硼原子的电子排布式为___________________。
(2)下列关于这两种晶体的说法,正确的是______________(填序号)
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体的B-N键均为共价键
d.两种晶体均为分子晶体
e.立方相氮化硼的晶体晶胞中,含有4个B原子,4个N原子
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___________,其结构与石墨相似却不导电,原因是________________________________。
(4)立方氮化硼和金刚石是等电子体,其晶胞如图所示,则处于晶胞顶点上的原子配位数为________________,若晶胞边长为361.5pm,则立方氮化硼的密度是______________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
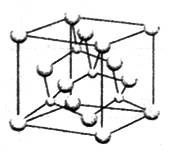
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1mol NH4BF4含有___________mol配位键。
答案
【答案】 (1). 1s22s22p1 (2). bce (3). 平面三角形 (4). 层状结构中没有自由移动的电子 (5). 4 (6). ![]() (7). 2
(7). 2
【解析】(1)在元素周期表中B是5号元素,基态硼原子的电子排布式为1s22s22p1。
(2)a项,立方相氮化硼中,N原子和B原子之间存在共价单键,所以该化合物中含有σ键不存在π键,故a错误;b项,六方相氮化硼层间为分子间作用力,作用力小,导致其质地软,故b正确;c项,非金属元素之间易形成共价键,所以N原子和B原子之间存在共价键,故c正确;d项,立方相氮化硼为空间网状结构,不存在分子,为原子晶体,故d错误;e项,由均摊法可知,立方相氮化硼的晶胞中含有4个B原子、4个N原子,e正确;故答案为:bce。
(3)六方相氮化硼晶体层内一个硼原子与相邻3个氮原子形成3个σ键,无孤电子对,其空间构型为平面三角形,其结构与石墨相似,但六方相氮化硼晶体的层状结构中没有自动移动的电子,故不导电。
(4)一个立方氮化硼晶胞中含有4个N原子和4个B原子,以B原子为中心,与B原子距离最近且等距离的N原子有4个,则处于晶胞顶点上的原子配位数为4;一个晶胞的质量为![]() g,晶胞的体积为
g,晶胞的体积为![]() cm3 = 361.5 pm×10-10cm/ pm,所以ρ =
cm3 = 361.5 pm×10-10cm/ pm,所以ρ = ![]() g·cm-3 =
g·cm-3 = ![]() g·cm-3。
g·cm-3。
(5)NH4BF4(氟硼酸铵)含有NH4+、BF4-离子,1个NH4+离子中含有1个配位键,1个BF4-离子中也含有1个配位键,故1 mol NH4BF4含有2 mol配位键。
点睛:本题考查了物质结构与性质,涉及基态原子的电子排布式书写、晶体与非晶体的判断、化学键、配位键、原子杂化方式的判断、微粒空间构型的判断、晶胞的有关计算等知识点,题目有一定难度。计算晶胞密度的方法:①首先找出晶胞;②确定晶胞内所有的原子或离子的种类和位置;③搞清每个原子或离子是完全在晶胞内部还是被不同晶胞共用;④把一个晶胞所有的原子或离子考虑共用后加起来,求的质量;⑤根据晶胞的几何形状计算其体积,乘以NA得到1mol晶胞的体积;⑥用第四步的质量除以第五步的体积(均为1mol)即为密度。
