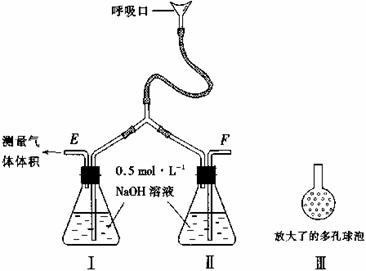
气体检验的方法:
(1)观察法:对于特殊颜色的气体如Cl2(黄绿色)、NO2(红棕色)、碘蒸气(紫红)可据此辨之。
(2)溶解法:根据溶于水的现象不同区分,如NO2和溴蒸气均为红棕色,但溶于水后NO2形成无色溶液;溴形成橙色溶液。
(3)褪色法:SO
2和CO
2可用品红溶液区分。
(4)氧化法:被空气氧化看变化,如NO的检验。
(5)试纸法:如石蕊试纸、醋酸铅试纸。
(6)星火发:适用于有助燃性或可燃性的气体检验,如O
2使带火星木条复燃;CH
4和C
2H
2的检验可点燃看现象;CH
4、CO、H
2则可根据其燃烧产物来判断。
常见气体的检验:
(1)H
2:无色、无味、可燃;①不纯点燃发出爆鸣声;②点燃纯H
2,火焰呈淡色,火焰上方罩一干燥烧杯,烧杯壁上有水珠生成:2H
2+O2

2H
2O
(2)O
2:无色无味、能使余烬木条复燃;
(3)Cl
2:黄绿色刺激性气体有毒;①使湿润淀粉碘化钾试纸变蓝:Cl
2+2KI=2KCl+I
2 I
2遇淀粉变蓝;②使湿润蓝色石蕊试纸先变红后变白:Cl
2+H
2O=HCl+HClO HClO强氧化性漂白作用;
(4)CO
2:无色无味无毒;①使燃着木条熄灭;②通入澄清石灰水变浑浊:CO
2+Ca(OH)
2=CaCO
3↓+H
2O
(5)CO:无色、无味、剧毒;点燃火焰呈蓝色,火焰上方罩一沾有石灰水液滴的烧杯,液滴变浑浊:
2CO+O
2
2CO
2 CO
2+Ca(OH)
2=CaCO
3↓+H
2O
(6)NO
2: 红棕色气体有刺激性气味、有毒,溶于水、水溶液呈酸性,能使紫色石蕊试液变红:3NO
2+H
2O=2HNO
3+NO
(7)NO:无色气体有毒;在空气中立即变为红棕色:2NO+O
2=2NO
2 (8)N
2: 无色无味无毒;能使燃着木条熄灭。
(9)SO
2:无色有刺激性气味、有毒;①通入品红溶液,品红褪色加热又恢复颜色;②使澄清石灰水变浑浊:
SO
2+Ca(OH)
2=CaSO
3+H
2O;
③使酸性高锰酸钾溶液褪色:5SO
2+2MnO
4-+2H
2O=2Mn
2++5SO
42-+4H
+ (10)HCl:无色刺激性气味;①能使湿润蓝色石蕊试纸变红:HCl=H
++Cl
-; ②用蘸浓氨水玻璃棒靠近冒白烟:NH
3+HCl=NH
4Cl;③气体通入HNO
3酸化的AgNO
3溶液,有白色沉淀生成:HCl+AgNO
3=AgCl↓+HNO
3 (AgCl不溶于HNO
3)
(11)H
2S:无色臭鸡蛋气味有毒;遇Pb(NO
3)
2 、(CH
3COO)
2Pb、CuSO
4溶液均产生黑色沉淀:Pb
2++H
2S=PbS↓+2H
+;2CH
3COO
-+Pb
2++H
2S=PbS↓+2CH
3COOH;Cu
2++H
2S=CuS↓+2H
+ (12)NH
3:无色刺激性气味;①遇湿润红色石蕊试纸变蓝:NH
3+H
2O

NH
3?H
2O

NH
4++OH
-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH
3+HCl==NH
4Cl
(13)CH
4:无色无味、可燃;点燃后火焰呈浅蓝色,火焰上方罩一干燥烧杯,烧杯壁上有水珠罩生成;罩一沾有石灰水液滴的烧杯,液滴变浑浊:CH
4+2O
2
CO
2+2H
2O CO
2+Ca(OH)
2==CaCO
3↓+H
2O
(14)C
2H
4: 无色稍有气味;①点燃,火焰明亮(少量黑烟):C
2H
4+3O
2
2CO
2+2H
2O ;②使KMnO
4(H
+)溶液褪色;③使溴水褪色:CH
2=CH
2+Br
2→CH
2Br-CH
2Br
(15)C
2H
2:无色无味;①点燃火焰明亮并伴有大量黑烟:2C
2H2+5O
2
4CO
2+2H
2O;②使KMnO
4(H
+)溶液褪色;③使溴水褪色:CH≡CH+2Br
2→CHBr
2-CHBr
2 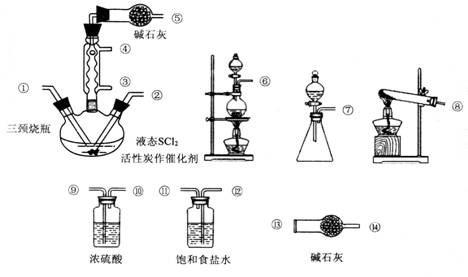 氯化亚砜(SOCl2)是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。实验室合成原理:SO2+C12+SCl2=2SOCl2,部分装置如下图所示,回答以下问题:
氯化亚砜(SOCl2)是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。实验室合成原理:SO2+C12+SCl2=2SOCl2,部分装置如下图所示,回答以下问题:

 2H2O
2H2O  2CO2 CO2+Ca(OH)2=CaCO3↓+H2O
2CO2 CO2+Ca(OH)2=CaCO3↓+H2O  NH3?H2O
NH3?H2O NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl
NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl  CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O
CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O  2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br
2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br  4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2
4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2  的检验;
的检验;  的检验;
的检验;  苯酚的检验。
苯酚的检验。