下列操作或装置能达到实验目的是( )
| 选项 | A | B | C | D |
| 操作或装置 |
|
|
|
|
| 目的 | 配制一定物质的量浓度溶液 | 分离Na2CO2溶液和CH3COOC2H5的混合物 | 做“白色”喷泉实验 | 用NaOH溶液滴定稀盐酸 |
A.A B.B C.C D.D
答案
【考点】U5:化学实验方案的评价;QB:实验装置综合.
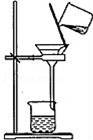
【分析】A.转移液体需要引流;
B.Na2CO2溶液和CH3COOC2H5的混合物分层;
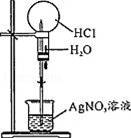
C.HCl与硝酸银溶液反应生成白色沉淀,烧瓶内气体减少,外压大于内压;
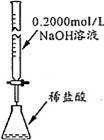
D.NaOH不能用酸式滴定管盛放.
【解答】解:A.转移液体需要引流,图中缺少玻璃棒,故A错误;
B.Na2CO2溶液和CH3COOC2H5的混合物分层,应选分液装置,而图中为过滤装置,故B错误;
C.HCl与硝酸银溶液反应生成白色沉淀,烧瓶内气体减少,外压大于内压,则图中装置可做白色”喷泉实验,故C正确;
D.NaOH不能用酸式滴定管盛放,应选碱式滴定管,故D错误;
故选C.