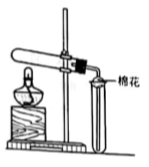
在自然界中硼元素常以硼砂的形式存在。硼砂的化学式为Na2B4O7・10H2O。用盐酸或碳酸处理硼砂便得到硼酸:
Na2B4O7・10H2O + 2H+ → 4H3BO3 + 2Na+ + 5H2O
(1)按上述反应式生产30g硼酸,需用多少克硼砂?
(2)为使上述反应式的的转化成为可能,需加入密度d = 1.12g・cm-3的25%盐酸多少mL?
(3)已知硼的配位数为3和4,试画出硼砂的结构式(2个硼是三配位,2个硼是四配位)。
答案
解析:前两小题是根据方程式进行运算的,第3小题要充分应用所给条件,联系已学的课本知识进行系逻辑思维。
解:(1)M (H3BO3) = 62g・mol-1 M (硼砂) = 382g・mol-1
m (硼砂)=  × 328g・mol-1 = 46.21g
× 328g・mol-1 = 46.21g
(2) m (HCl) = ![]() × 36.5g・mol-1= 8.83g
× 36.5g・mol-1= 8.83g
V(HCl) = ![]() ÷ 1.12 g・mol-1 =31.54 mL
÷ 1.12 g・mol-1 =31.54 mL
(3)Na2B4O7・10H2O = [Na(H2O)4]2[B4O5(OH)4]
[B4O5(OH)4]2-结构为: