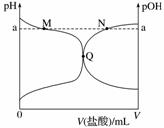
室温下,将0.10 mol·L-1盐酸滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列说法正确的是( )
A.M点所示溶液中c(NH![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
B.N点所示溶液中c(NH![]() )>c(Cl-)
)>c(Cl-)
C.Q点消耗盐酸的体积等于氨水的体积
D.M点和N点所示溶液中水的电离程度相同
答案
答案 D
解析 A中所示的式子必须在加入的盐酸的物质的量与氨水的物质的量相等时才满足,M点显然不成立;B中,N点,盐酸已经明显过量了,c(Cl-)>c(NH![]() );C中,Q点处溶液为中性,但是此时消耗盐酸的体积比氨水的体积小;D中,M点与N点对应的pH与pOH相同,所以对水的电离程度抑制作用相同,所以水的电离程度相同。
);C中,Q点处溶液为中性,但是此时消耗盐酸的体积比氨水的体积小;D中,M点与N点对应的pH与pOH相同,所以对水的电离程度抑制作用相同,所以水的电离程度相同。

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。