 已知某放热热反应在1L的密闭容器中进行反应。保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如下图所示:
已知某放热热反应在1L的密闭容器中进行反应。保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)写出该反应的化学方程式 ;
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、
vⅢ(A)从小到大排列次序为 ;
(3)由第二次平衡到第![]() 三次平衡,平衡移动的方向是 (填“正向移动”“逆向移动”“不移动”),改变的条件是 ;
三次平衡,平衡移动的方向是 (填“正向移动”“逆向移动”“不移动”),改变的条件是 ;
(4)在Ⅰ阶段20min时,若在恒温恒压条件下再向该体系中通入3mol A,1mol B,2 molC,则化学平衡 .(填“正向移动”“逆向移动”“不移动”或“无法确定”).
答案
(1)A(g)+3B(g) ![]() 2C(g)
2C(g)
(2)vⅢ(A)<vⅡ(A)<vⅠ(A)
(3)正向移动 降低温度
(4)逆向移动 [解析]因为该温度下化学平衡常数K=![]() 恒压条件下通入3mol A,1mol B,2 molC,体积增大到原来2倍,
恒压条件下通入3mol A,1mol B,2 molC,体积增大到原来2倍,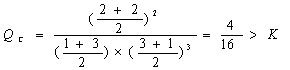 所以平衡逆向移动。
所以平衡逆向移动。
