锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为 6C +xLi++xe-===LixC6。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
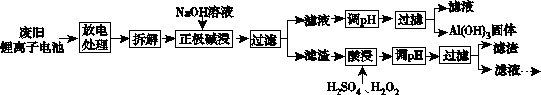

回答下列问题:
(1)Co元素在元素周期表中的位置为 。
(2)“酸浸”一般在80 ℃下进行,写出该步骤中发生的一个主要氧化还原反应的化学方程式__________;可用盐酸代替H2SO4和H2O2的混合液,但缺点是__________________。
(3)写出“沉钴”过程中发生反应的离子方程式_________![]() _____________________。
_____________________。
(4)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池的正极反应方程式_____________________________。
(5)在整个回收工艺中,可回收到的金属化合物有(填化学式)____________。
答案
(1)第四周期Ⅷ族
(2)2LiCoO2+3H2SO4+H2O2Li2SO4+2CoSO4+O2↑+4H2O
有氯气生成,污染较大
(3) Co2++2HCO3—===CoCO3↓+H2O+CO2↑
(4)Li1-xCoO2+xLi++xe-===LiCoO2
(5) Al(OH)3、CoCO3、Li2SO4(错1个 不给分)


