汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.根据下列示意图回答有关问题:
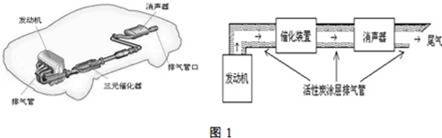

(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJ•mol﹣1,其能量变化示意图如下:
![]()
![]()
则NO中氮氧键的键能为 kJ•mol﹣1;
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)⇌N2(g)+xCO2 (g)△H=﹣b kJ•mol﹣1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是 A;
A.增加排气管长度 B.增大尾气排放口
C.升高排气管温度 D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)⇌N2(g)+2CO2(g).
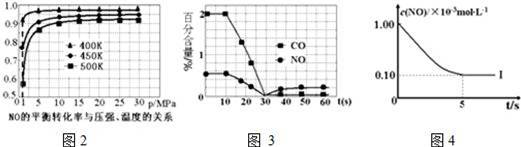

①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是 ;
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是 ;
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
| 实验编号 | T(K) | NO初始浓度 (mol•L﹣1) | CO初始浓度 (mol•L﹣1) | 催化剂的比表面积(m2/g) |
| Ⅰ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 82 |
| Ⅱ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
| Ⅲ | 450 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
根据坐标图4,计算400K时该反应的平衡常数为 .
答案
【考点】反应热和焓变;化学平衡的影响因素;化学平衡的计算.
【分析】(1)△H=反应物的键能总和﹣生成物的键能总和;
(2)根据△H﹣T△H<0来判断反应的自发性;
(3)A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,对平衡无影响;
B.增大尾气排放口,对反应速率和平衡不产生影响;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化;
D.添加合适的催化剂,加快化学反应速率,对平衡无影响;
(4)①综合考虑NO的转化率和成本;
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;
③结合表格中的浓度,利用三段法列出400K时平衡浓度,带入平衡常数表达式计算;根据外界条件对化学反应速率和化学平衡的影响判断.
【解答】解:(1)设NO中氮氧键的键能为x,
△H=反应物的键能总和﹣生成物的键能总和=kJ•mol﹣1﹣2×x=180kJ•mol﹣1,解得x=632 kJ•mol﹣1,
故答案为:632;
(2)2CO(g)=2C(s)+O2(g)(△H>0、△S<0)是一个焓增、熵减的反应,任何情况下不能自发进行,所以无法消除CO的污染,
故答案为:不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0则△G>0;
(3)xC(s)+2NOx(g)⇌N2(g)+xCO2 (g)△H=﹣b kJ•mol﹣1.此反应为放热反应,
A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,故A正确;
B.增大尾气排放口,对反应速率和平衡不产生影响,故B错误;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化,故C错误;
D.添加合适的催化剂,加快化学反应速率,故D正确;
故答案为:AD;
(4)①由图2可知,等压条件下,温度越低,NO的转化率越高,因此温度选400K,同温下,NO的转化率随着温度的升高变化不大,所以选用较为经济的1MPa,
故答案为:400K,1MPa:
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;证明反应未达到催化剂工作温度(或尚未达到反应的温度);
故答案为:尚未达到催化剂工作温度(或尚未达到反应的温度);
③设400K达到平衡状态时,则
2NO(g)+2CO(g)⇌N2(g)+2CO2(g).
初始浓度(10﹣3mol•L﹣1):1 3.60 0 0
转化浓度(10﹣3mol•L﹣1):0.9 0.9 0.45 0.9
平衡浓度(10﹣3mol•L﹣1):0.1 2.7 0.45 0.9
K=![]()
![]() =5000L•mol﹣1,
=5000L•mol﹣1,
故答案为:5000L•mol﹣1.
