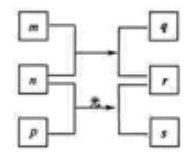
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
答案
【答案】C
【解析】
试题分析:短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,则Z是氯元素,n是Cl2;0.01 mol·L–1 r溶液的pH为2,说明r是一元强酸,Cl2与两种元素组成的化合物反应会产生两种化合物,其中一种r是HCl,另一种物质q的水溶液具有漂白性,则说明W是H元素;m是H2O, q是HClO;两种元素组成的化合物p与Cl2光照反应产生HCl,同时产生s,s通常是难溶于水的混合物,根据转化关系图可知p是甲烷,则s可能是CH3Cl、CH2Cl2、CHCl3、CCl4中的几种物质。因此X是碳元素,Y是氧元素。A.根据元素周期律的原子半径变化规律:同一周期的元素,原子序数越大原子半径越小,同一主族的元素,原子核外电子层数越多,原子半径越大,则原子半径的大小W<Y<X,错误;B.同一周期元素,随着原子序数的增大,自左向右元素的非金属性逐渐增强,同主族元素自上而下,随着原子序数的增大,元素的非金属性逐渐减弱,则元素的非金属性Y>Z>X,错误;C.Y元素的氢化物有H2O和H2O2,二者在常温常压下都为液态,正确;D.X的最高价氧化物的水化物是碳酸,该物质是二元弱酸,不是强酸,错误。
【考点定位】考查元素周期表、元素周期律的应用及和无机框图题推断的知识。
【名师点睛】元素周期表、元素周期律是学习化学的工具和基本规律。元素周期表反映了元素的原子结构、元素的性质及相互转化关系的规律,是根据元素周期律的具体表现形式,元素周期律是元素周期表排布的依据。元素的原子半径、元素的化合价、元素的金属性、非金属性、原子核外电子排布都随着原子序数的递增而呈周期性的变化。同一周期的元素原子核外电子层数相同,从左到右原子序数逐渐增大;同一主族的元素,原子最外层电子数相同,从上到下原子核外电子层数逐渐增大。原子核外电子排布的周期性变化是元素周期律变化的原因,掌握元素的单质及化合物的结构、反应条件、物质的物理性质、化学性质等是进行元素及化合物推断的关键。本题难度较大,常由于物质的某个性质未掌握好导致失误、失分。
