用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。反应A: 4HCl+O2 ![]() 2Cl2+2H2O。
2Cl2+2H2O。
(1)已知:i 反应A中, 4mol HCI被氧化,放出115.6kJ的热量。
ii ![]()
①H2O的电子式是_______________。
②反应A的热化学方程式是____________________________________________________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),
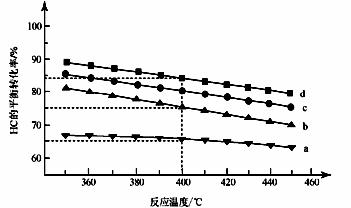
分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是__________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度高低与投料比多少的关系是______________________________。
400oC
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数__________。
答案
【答案】(1)①H:O:H (2分) ②4HCl(g)+O2(g)![]() 2Cl2+2H2O(g) △H=-115.6kJ/mul (2分)
2Cl2+2H2O(g) △H=-115.6kJ/mul (2分)
③32或31.9kJ (1分) 强(1分) (2)①4:1 (1分) ②投料比越小时对应的温度越低(1分) ③30.8% (2分)
 考点:热化学方程式、外界条件对平衡状态的影响以及可逆反应的有关计算
考点:热化学方程式、外界条件对平衡状态的影响以及可逆反应的有关计算
