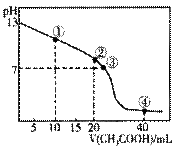
25℃时,向20.00 mL的NaOH溶液中逐滴加入某浓度的CH3COOH溶液。滴定过程中,溶液的pH与滴入CH3COOH溶液的体积关系如图所示,点②时NaOH溶液恰好被中和。则下列说法中,错误的是( )
A.CH3COOH溶液的浓度为0.1 mol·L-1
B.图中点①到点③所示溶液中,水的
电离程度先增大后减小
C.点④所示溶液中存在:
(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-)
D.滴定过程中会存在:
c(Na+)> c(CH3COO-)=c(OH-)> c(H+)
答案
【答案】C
【解析】
试题分析:A、图像分析氢氧化钠溶液的浓度为0.1mol/L,②点时氢氧化钠溶液恰好被中和消耗醋酸的溶液20ml,则醋酸浓度为0.1mol/L,正确,不选A;B、图中①点到③点所示溶液中随着滴入醋酸反应,水的电离被抑制程度减小,即水的电离程度增大,恰好反应后继续滴加醋酸,对水的电离起到抑制作用,图中①到③所示的溶液中水的电离程度先增大后减小,正确,选B;C、④点所示溶液是醋酸和醋酸钠溶液,(CH3COOH)+ c(CH3COO-) = 2c(Na+),电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),错误,不选C;D、滴定过程中的某点,醋酸钠和氢氧化钠混合溶液中会有c(Na+)> c(CH3COO-)=c(OH-)> c(H+),正确,选D。
酸碱中和滴定类试题解题的难点在于整个过程是一个动态过程,我们要将一个动态过程转化为一个静态的点进行分析,然后运用上一考点的知识进行解决。这类图像题在解题过程还可以以两个关键点进行分段分析,一是滴定终点,此时酸碱恰好中和,为单一盐溶液,只需考虑水解;另一为pH=7的点,此时溶液呈中性,从守恒角度进行考虑。

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。