氮化硼( BN)是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到BN和火箭高能燃料及有机合成催化剂BF3的过程如下:
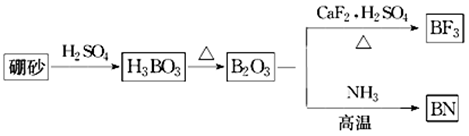
(1)写出由B203制备BF3的化学方程式 ,BF3中,
B原子的杂化轨道类型为_ _。[来源:Z-x-x-k.Com]
(2)已知:硼酸的电离方程式为H3B03 +H20 ![]() [
[![]() B(OH)4] - +H+,试依据上述反应写出
B(OH)4] - +H+,试依据上述反应写出[来源:学科网][ Al( OH)4] -的结构式_ ___,并推测1mol NH4BF4(氟硼酸铵)中含有__ __个配位键。
(3)由12个硼原子构成如图1的结构单元,硼晶体的熔点为1873℃,则硼晶体的1个结构单元中含有__ __ 个B-B键。
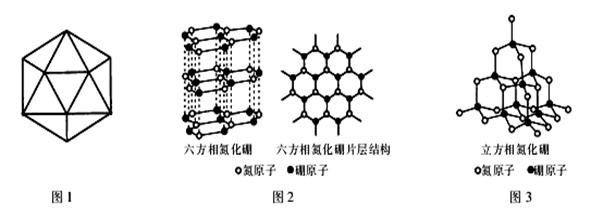
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼(晶体结构如图2)是通常存在的稳定相可作高温润滑剂。立方相氮化硼(晶体结构如图3)是超硬材料,有优异的耐磨性。
①关于这两种晶体的说法,不正确的是____(填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B-N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体结构与石墨相似却不导电,原因是__ __。
(5)一种硼酸盐的阴离子为B3O6n-, B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数);
_________________________________________________________。
答案
(15分)(1)![]()
sp2 (1分);(2) ![]() (2分)
(2分)![]() (1分)
(1分)
(3)30 (2分)(4)①ad (2分); ②立方氮化硼晶体内无自由移动的电子 (2分)
(5) 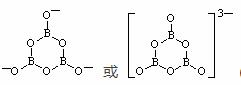 (3分)
(3分)
