硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。常温下该物质在空气中易与水和二氧化碳反应,生成铜的碱式盐,使晶体变成绿色的粉末。下面为硫酸四氨合铜晶体的制备以及NH3和SO42-质量百分数的测定实验。
步骤一:硫酸四铵合铜晶体的制备
发生反应为:CuSO4 + 4NH3·H2O = [Cu(NH3)4]SO4·H2O + 3H2O 。现取10 g CuSO4·5H2O溶于14 mL水中,加入20 mL浓氨水, 沿烧杯壁慢慢滴加95%的乙醇。静置析出晶体后,减压过滤,晶体用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在60 ℃左右小心烘干。
步骤二:NH3的质量百分数的测定(装置如图所示)
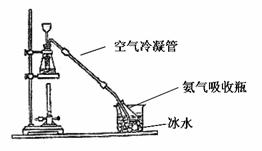
称取0.250 g 样品,放入250 mL锥形瓶中,加80 mL水溶解。在另一锥形瓶中,准确加入30 mL 0.500 mol•L-1 HCl标准溶液,放入冰水浴中。从漏斗中加入15 mL 10% NaOH溶液,加热样品,保持微沸状态 1小时左右。蒸馏完毕后,取出插入HCl 溶液中的导管,用蒸馏水冲洗导管内外,洗涤液收集在氨吸收瓶中,从冰水浴中取出吸收瓶,加 2 滴酸碱指示剂,用0.500 mol•L-1的NaOH标准溶液滴定,用去NaOH标准溶液22.00 mL。
步骤三:SO42-质量百分数的测定
称取试样0.600 g置于烧杯中,依次加入蒸馏水、稀盐酸、BaCl2溶液,水浴加热半小时。过滤,用稀硫酸洗涤。取下滤纸和沉淀置于已恒重的坩埚中在800-850℃灼烧至再次恒重,得到固体0.699 g。
(1)步骤一加入95%乙醇的作用为____________________________。此步骤进行两次洗涤操作,用乙醇与乙醚的混合液淋洗的目的为____________________。不采用蒸发浓缩、冷却结晶的方法制备硫酸四氨合铜晶体的原因为__________________。
(2)步骤二装置中15 mL 10% NaOH溶液加热样品,保持微沸状态1小时左右的目的是__________。通过此步骤测定NH3的质量百分数为_________________。此实验装置,如不使用空气冷凝管和冰水浴将使氨气的测定结果_______________(“偏高”、“不变”或“偏低”)。
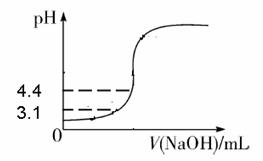
(3)步骤二中,根据酸碱中和滴定曲线分析,此实验中所加入的酸碱指示剂为___________。
A.甲基橙 B.甲基红 C.酚酞
(4)步骤三中用稀硫酸洗涤的目的是_______________(用必要的方程式和文字说明)。该步骤中灼烧过程如果温度过高可生成一种有害气体和一种可溶于水的盐,写出该反应的化学方程式_________。
答案
【答案】(1)降低硫酸四氨合铜晶体的溶解度,有利于晶体析出。(1分) 下一步烘干温度较低,利用乙醇与乙醚易挥发的性质,得到较干燥的硫酸四氨合铜晶体,大量减少下一步烘干所用时间。(1分) 硫酸四氨合铜蒸发浓缩过程,受热分解可以生成NH3 (2分)
(2)将氨全部蒸出,从而得到准确的测量结果(2分) 27.2 % (2分) 偏高(2分)
(3)B(1分) (4)BaSO4(s) ![]() Ba2+(aq) + SO42—(aq),洗净杂质的同时,SO42—浓度升高使BaSO4的沉淀溶解平衡逆向移动,减少BaSO4的溶解。(2分) BaSO4 + 4C
Ba2+(aq) + SO42—(aq),洗净杂质的同时,SO42—浓度升高使BaSO4的沉淀溶解平衡逆向移动,减少BaSO4的溶解。(2分) BaSO4 + 4C ![]() 4CO↑+ BaS(2分)
4CO↑+ BaS(2分)
【解析】
试题分析:(1)四氨合铜晶体在有机溶剂中的溶解度小,所以步骤一加入95%乙醇的作用为降低硫酸四氨合铜晶体的溶解度,有利于晶体析出;由于乙醇易挥发,而下一步烘干温度较低,所以可利用乙醇与乙醚易挥发的性质,得到较干燥的硫酸四氨合铜晶体,大量减少下一步烘干所用时间;由于硫酸四氨合铜蒸发浓缩过程,受热分解可以生成NH3,所以不采用蒸发浓缩、冷却结晶的方法制备硫酸四氨合铜晶体。
(2)氨气极易溶于水,所以保持微沸状态 1小时左右的目的是将氨全部蒸出,从而得到准确的测量结果;与盐酸反应的氢氧化钠是0.022L×05mol/L=0.011mol,则吸收氨气的盐酸的物质的量是0.03L×0.5mol/L-0.011mol=0.004mol,即氨气的物质的量是0.004mol,所以NH3的质量百分数为![]() =27.2 %;如不使用空气冷凝管和冰水浴,则导致盐酸挥发,消耗氢氧化钠溶液的体积减小,所以将使氨气的测定结果偏高。
=27.2 %;如不使用空气冷凝管和冰水浴,则导致盐酸挥发,消耗氢氧化钠溶液的体积减小,所以将使氨气的测定结果偏高。
(3)根据图像可知发生突变时溶液的pH大于4.4而小于7,甲基橙的变色范围是3.1~4.4,酚酞是8.2~10.,因此应该选择甲基红,答案选B。
(4)由于BaSO4(s)![]() Ba2+(aq) + SO42—(aq),洗净杂质的同时,SO42—浓度升高使BaSO4的沉淀溶解平衡逆向移动,减少BaSO4的溶解,所以步骤三中用稀硫酸洗涤;灼烧过程如果温度过高可生成一种有害气体和一种可溶于水的盐,气体是CO,所以该反应的化学方程式为BaSO4 + 4C
Ba2+(aq) + SO42—(aq),洗净杂质的同时,SO42—浓度升高使BaSO4的沉淀溶解平衡逆向移动,减少BaSO4的溶解,所以步骤三中用稀硫酸洗涤;灼烧过程如果温度过高可生成一种有害气体和一种可溶于水的盐,气体是CO,所以该反应的化学方程式为BaSO4 + 4C ![]() 4CO↑+ BaS。
4CO↑+ BaS。
考点:考查物质制备、含量测定实验方案设计与探究


