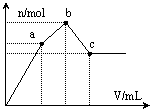
镁铝合金5.1g溶于300mL 2mol/L盐酸中,标准状况下放出气体体积为5.6L,向反应后的溶液中加入500mLNaOH溶液充分反应,最终产生白色沉淀.下列有关说法不正确的是( )
A.5.1g镁铝合金中含有镁、铝的质量分别为2.4g、2.7g
B.溶解5.1g镁铝合金![]() 时,剩余盐酸的物质的量为0.1mol
时,剩余盐酸的物质的量为0.1mol
C.生成白色沉淀的最大质量为13.6g
D.若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2mol/L
答案
【答案】D
【解析】
试题分析:盐酸中n(HCl)=300×10-3×2mol=0.6mol,H2中氢原子物质的量n(H)=5.6×2/22.4mol=0.5mol<0.6mol,说明盐酸过量,合金全部溶解,设金属镁物质的量为xmol,金属铝为ymol,则有24x+27y=5.1,根据得失电子数目守恒,2x+3y=5.6×2/22.4,两式联立解得:x=y=0.1mol,A、根据上述分析,合金中两种金属的质量分别是2.4g、2.7g,故说法正确;B、剩余盐酸的物质的量为300×10-3×2-0.1×2-0.1×3mol=0.1mol,故说法正确;C、根据物质的分析,沉淀最大,Mg全部转化成Mg(OH)2,Al全部转化成Al(OH)3,沉淀的质量等于合金的质量+OH-的质量,而OH-的物质的量等于合金失去电子物质的量等于氢得到电子的物质的量,因![]() 此沉淀的质量为=5.1+5.6×2×17/22.4g=13.6g,故说法正确;D、根据溶液呈现电中性,反应后的溶质NaCl、NaAlO2,即n(Na+)=n(Cl-)+n(AlO2-)=300×10-3×2+0.1mol=0.7mol,因此消耗氢氧化钠的体积为0.7/500×10-3mol·L-1=1.4mol·L-1。
此沉淀的质量为=5.1+5.6×2×17/22.4g=13.6g,故说法正确;D、根据溶液呈现电中性,反应后的溶质NaCl、NaAlO2,即n(Na+)=n(Cl-)+n(AlO2-)=300×10-3×2+0.1mol=0.7mol,因此消耗氢氧化钠的体积为0.7/500×10-3mol·L-1=1.4mol·L-1。
考点:考查化学计算等知识。

 (纯氧中发出耀眼的白光)
(纯氧中发出耀眼的白光) (Al2S3在溶液中完全双水解)
(Al2S3在溶液中完全双水解)
 (AlN与水反应生成Al(OH)3和NH3↑)
(AlN与水反应生成Al(OH)3和NH3↑) 




 ,
, ,所以根据得失电子守恒可知:
,所以根据得失电子守恒可知: ,利用此关系可以方便地进行有关计算。
,利用此关系可以方便地进行有关计算。