柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4•7H2O)通过下列反应制备:FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O 下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L﹣1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
(1)制备FeCO3时,选用的加料方式是 (填字母),原因是 .
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是 .
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应.①铁粉的作用是 .②反应结束后,无需过滤,除去过量铁粉的方法是 .
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是
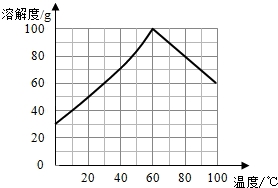
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3) 出发,先制备绿矾,再合成柠檬酸亚铁.请结合如图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4•7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应, ”
,得到FeSO4•7H2O 晶体.
答案
【考点】铁的氧化物和氢氧化物;铁盐和亚铁盐的相互转变;硫酸亚铁的制备.
【专题】压轴题;几种重要的金属及其化合物.
【分析】(1)利用Na2CO3溶液和FeSO4溶液反应制备FeCO3,由于Na2CO3溶液碱性很强,可能会生成Fe(OH)2沉淀,为避免生成Fe(OH)2沉淀,如果将Na2CO3加入FeSO4溶液中,Fe2+是过量的,并且FeSO4溶液为酸性,Fe2+不易沉淀.因此,CO32﹣容易与Fe2+结合为沉淀析出,因此应将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中;
(2)判断沉淀是否洗净的方法:取最后一次洗涤的滤液,检测滤液中是否存在未洗涤干净的杂质.首先要弄清沉淀上的杂质是什么,然后再去检测里面的离子.本题中FeCO3的制备是用Na2CO3溶液和FeSO4溶液的反应,因而沉淀表面可能会有Na2SO4杂质,因而应该检验最后一次洗涤滤液中是否含有SO42﹣,即该题便转化成SO42﹣的检验;
(3)因+2的Fe元素易被空气中的氧气氧化,制备柠檬酸亚铁过程中应尽量避免与氧气接触.加入铁粉的目的就是与柠檬酸反应产生H2,形成一个无氧的环境.除去过量的铁粉可直接加入适量的柠檬酸,反应也生成了需要的产品柠檬酸亚铁,不会引入杂质.
(4)最后的溶液经浓缩形成柠檬酸亚铁的饱和溶液,要得到尽可能多的柠檬酸亚铁晶体,可加入无水乙醇,可以降低柠檬酸亚铁的溶解度,从而获得更多的产品.
(5)由硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 )制备FeSO4•7H2O晶体,要弄清楚流程中每一步的原理和注意事项.向烧渣中加入足量的稀硫酸,Fe2O3、Al2O3均会与硫酸反应,分别生成Fe2(SO4)2和Al2(SO4)2,SiO2不反应,先过滤把SiO2除去,然后向滤液中加入足量的铁粉,将Fe3+转化成Fe2+,根据金属离子沉淀的pH值,然后通过滴加NaOH溶液调节pH至5.0把Al3+除去,过滤,即得到FeSO4溶液,再根据绿矾溶解度曲线,60℃时绿矾的溶解度最大,可加热浓缩到60℃的饱和溶液,然后放在冰水中冷却,冷却结晶至0℃,此时析出的晶体是最多的,之后过滤,洗涤,低温烘干.
【解答】解:(1)利用Na2CO3溶液和FeSO4溶液反应制备FeCO3,由于Na2CO3溶液碱性很强,可能会生成Fe(OH)2沉淀,如果将Na2CO3加入FeSO4溶液中,Fe2+是过量的,并且FeSO4溶液为酸性,Fe2+不易沉淀.因此,CO32﹣容易与Fe2+结合为沉淀析出,因此为避免生成Fe(OH)2沉淀,应将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中;
故答案为:c,避免生成Fe(OH)2沉淀;
(2)判断沉淀是否洗净的方法:取最后一次洗涤的滤液,检测滤液中是否存在未洗涤干净的杂质.首先要弄清沉淀上的杂质是什么,然后再去检测里面的离子.本题中FeCO3的制备是用Na2CO3溶液和FeSO4溶液的反应,因而沉淀表面可能会有Na2SO4杂质,因而应该检验最后一次洗涤滤液中是否含有SO42﹣,即该题便转化成SO42﹣的检验.具体操作为:取最后一次的洗涤滤液1~2 mL 于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净;
故答案为:取最后一次的洗涤滤液1~2 mL 于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净;
(3)因+2的Fe元素易被空气中的氧气氧化,制备柠檬酸亚铁过程中应尽量避免与氧气接触.加入铁粉的目的就是与柠檬酸反应产生H2,形成一个无氧的环境.除去过量的铁粉可直接加入适量的柠檬酸,反应也生成了需要的产品柠檬酸亚铁,不会引入杂质;
故答案为:防止+2价的铁元素被氧化,加入适量柠檬酸让铁粉反应完全;
(4)最后的溶液经浓缩形成柠檬酸亚铁的饱和溶液,要得到尽可能多的柠檬酸亚铁晶体,可加入无水乙醇,可以降低柠檬酸亚铁的溶解度,从而获得更多的产品;
故答案为:降低柠檬酸亚铁在水中的溶解量,有利于晶体析出;
(5)由硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 )制备FeSO4•7H2O晶体,要弄清楚流程中每一步的原理和注意事项.向烧渣中加入足量的稀硫酸,Fe2O3、Al2O3均会与硫酸反应,分别生成Fe2(SO4)2和Al2(SO4)2,SiO2不反应,先过滤把SiO2除去,然后向滤液中加入足量的铁粉,将Fe3+转化成Fe2+,根据金属离子沉淀的pH值,然后通过滴加NaOH溶液调节pH至5.0把Al3+除去,过滤,即得到FeSO4溶液,再根据绿矾溶解度曲线,60℃时绿矾的溶解度最大,可加热浓缩到60℃的饱和溶液,然后放在冰水中冷却,冷却结晶至0℃,此时析出的晶体是最多的,之后过滤,洗涤,低温烘干;
故答案为:过滤向反应液中加入足量的铁粉,充分搅拌后,滴加NaOH溶液调节反应液的pH约为5,过滤或“过滤,向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体,向固体中加入足量稀硫酸至固体完全溶解,再加入足量的铁粉,充分搅拌后,过滤;(滴加稀硫酸酸化,)加热浓缩得到60℃饱和溶液,冷却至0℃结晶,过滤,少量冰水洗涤,低温干燥.
【点评】本题考查了学生在新情境下物质的制备实验中基本的实验技能和对教材相关实验的理解的迁移能力,中档题难度偏大,掌握物质性质和实验技能是解题关键.