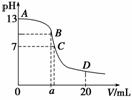
25 ℃时,在20 mL 0.1 mol·L-1 NaOH溶液中加入0.2 mol·L-1 CH3COOH溶液,所加入溶液
的体积(V)和混合液中pH变化关系的曲线如下图所示,若B点的横坐标a=10,下列分析的结论正确的是( )
A.在B点有:c(Na+)=c(CH3COO-)
B.对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
D.D点时,c(CH3COO-)+c(CH3COOH)=c(Na+)
答案
答案 C
解析 B点正好生成CH3COONa溶液。A项,B点c(Na+)>c(CH3COO-);B项,当接近B点时,此时,c(Na+)>c(CH3COO-)>c(OH-)>c(H+);D项,D点是CH3COOH和CH3COONa的等量混合溶液,此时c(CH3COO-)+c(CH3COOH)=2c(Na+)。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L