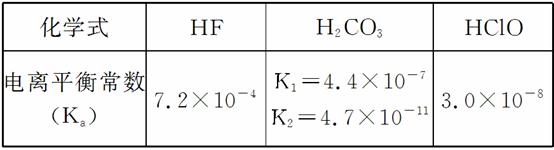
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25 ℃时,有关物质的电离平衡常数如下表所示:
(1)将浓度为0.1 mol·L-1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是________。
A.c(H+) B.c(H+)·c(OH-)
C.![]() D.
D.![]()
(2)25 ℃时,在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是________。
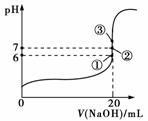
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F-)-c(Na+)=9.9×10-7 mol·L-1
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20 mL,此时溶液中c(F-)<c(Na+)=0.1 mol·L-1
(3)物质的量浓度均为0.1 mol·L-1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液。依据数据判断pH由大到小的顺序是__________________。
(4)Na2CO3溶液显碱性是因为CO![]() 水解的缘故,请设计简单的实验事实证明之__________________。
水解的缘故,请设计简单的实验事实证明之__________________。
(5)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H—O—F。HFO与水反应得到HF和化合物A,每生成1 mol HF转移________mol电子。
答案
解析:(1)加水稀释能促进氢氟酸的电离,溶液中氢离子浓度降低,故A错误;温度不变,水的离子积常数不变,故B错误;溶液中氢离子浓度和氢氟酸浓度都降低,该分式中都乘以氟离子浓度得氢氟酸的电离常数除以负离子浓度,电离常数不变,负离子浓度减小,所以其比值增大,故C正确;溶液中氢氧根离子浓度增大,氢离子浓度减小,故D正确。(2)A.酸能抑制水的电离,含有弱根离子的盐能促进水的电离,故错误。B.c(F-)-c(Na+)=c(H+)-c(OH-),故正确。C.溶液呈中性,氢离子浓度等于氢氧根浓度,所以氟离子浓度等于钠离子浓度,故正确。D.③点时V=20 mL,溶液呈碱性,根据溶液呈电中性知,钠离子浓度大于氟离子浓度,故错误。(3)根据相应酸的酸性强弱判断,氢氟酸的酸性大于碳酸的,碳酸的酸性大于次氯酸的,所以顺序为①④②③(或①>④>②>③,用物质名称表示也对)。(4)在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅。(5)HFO与水反应生成氢氟酸和双氧水,每生成1 mol HF转移2 mol电子。
答案:(1)CD (2)BC
(3)①④②③(或①>④>②>③,用物质名称表示也对)
(4)在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅
(5)2

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。