下列说法正确的是( )
A.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
B.25 ℃、101 kPa时,1 mol S和2 mol S的燃烧热不相等
C.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能
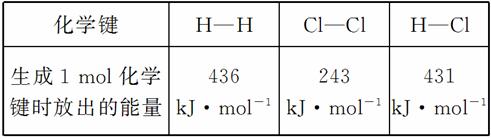
则![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g) ΔH=-183 kJ·mol-1
Cl2(g)===HCl(g) ΔH=-183 kJ·mol-1
D.任何化学反应都伴随着能量的变化
答案
解析:判断反应是否自发应用复合判据,A项错误;燃烧热不随物质的量的变化而变化,B项错误;根据表中数据可得H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ·moI-1,C项错误。
答案:D
