工业上用重铬酸钠(Na2Cr2O7)给晶后的母液(含少量杂质Fe3+生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图所示:
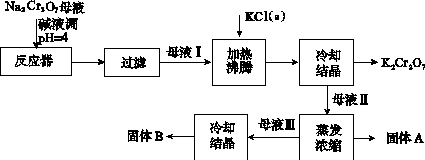
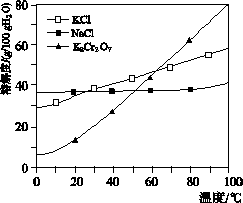
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为____________________________________________。通过冷却结晶析出大量K2Cr2O2的原因是__________________________________________________________。
(2)向Na2Cr2O7母液中加碱液调pH的目的是________________________________________。
(3)固体A主要为________(填化学式)。固体B主要为________(填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液______(填“Ⅰ”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗最低。
答案
(1)Na2Cr2O7+2KCl===K2Cr2O7+2NaCl 低温下K2Cr2O7溶解度远小于其他组分,随温度的降低,K2Cr2O7溶解度明显减小(合理即可)
(2)除去Fe3+
(3)NaCl K2Cr2O7
(4)Ⅱ
[解析] (1)利用流程图知向母液Ⅰ(溶质为Na2Cr2O7)中加入KCl(s)固体后得到K2Cr2O7,由此可知由Na2Cr2O7生成K2Cr2O7的反应的方程式为Na2Cr2O7+2KCl===K2Cr2O7+2NaCl;再结合溶解度曲线图可知该反应发生的原因是K2Cr2O7的溶解度受温度影响变化大,并且低温时溶解度远比其他组分小,将反应后的热溶液降温可使K2Cr2O7结晶析出。(2)pH=4时,Fe3+可完全转化为Fe(OH)3沉淀,通过过滤可进行固液分离,因此向Na2Cr2O7母液中加碱调节pH=4的目的是除去Fe3+。(3)利用(1)中反应方程式和溶解度曲线知,母液Ⅱ中主要含有NaCl和少量K2Cr2O7,再结合K2Cr2O7在高温时溶解度大可知将母液Ⅱ蒸发浓缩得到固体A应是析出NaCl固体,母液Ⅲ为高温下不饱和的K2Cr2O7溶液,再冷却结晶得到固体B应是K2Cr2O7。(4)洗涤固体A(NaCl)的洗涤液中含有K2Cr2O7,因此将回收液转移到母液Ⅱ中可提高K2Cr2O7的产率,同时降低能耗。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L