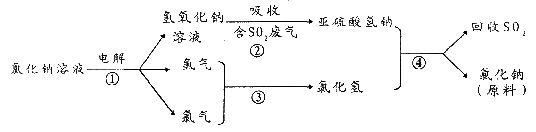
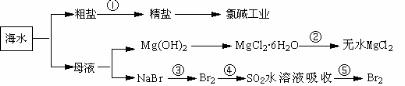
从海水中可提取各种化工原料,下图是工业上对海水的几项综合利用的示意图:

(1)在实验室进行过滤所需要玻璃仪器为______________。
(2)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液。
则加入试剂的顺序是(填编号)______
(3)电解饱和食盐水时,与电源正极相连的电极上发生的反应为_______;与电源负极相连的电极附近溶液的pH_______(填“变大”、“变小”和“不变”)
(4)Mg(OH)2中加入盐酸后,要获得MgCl2・6H2O晶体,需要进行的实验操作依次为_____
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(5)用相同电量分别电解无水MgCl2和饱和食盐水时,当生成1molMg的同时,生成NaOH的物质的量是________mol。
答案
(1)漏斗、烧杯、玻璃棒 (2)CBDA或BCDA (3)2Cl-2e=Cl2 变大
(4)DEC (5)2mol


 H2↑+Cl2↑+2NaOH 离子交换膜法制碱技术,具有设备占地面积小、能连续生产、生产能力大、产品质量高、能适应电流波动、能耗低、污染小等优点,是氯碱工业发展的方向。
H2↑+Cl2↑+2NaOH 离子交换膜法制碱技术,具有设备占地面积小、能连续生产、生产能力大、产品质量高、能适应电流波动、能耗低、污染小等优点,是氯碱工业发展的方向。