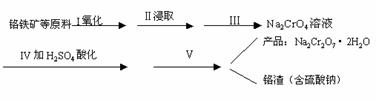
一真空密![]() 闭容器中盛有amolA,加热到200℃时发生如下反
闭容器中盛有amolA,加热到200℃时发生如下反
![]()
数为M%。若在同一温度和同一容器中,最初投入的是2amolA,反应平衡时,A所占体积分数为N%。则M和N的正确![]() 关系是
关系是
A.M>N B.M<N C.M=N D.无法比较
答案
【答案】D
【解析】在同温、同体积条件下,反应物投入的量由amol增加到2amol,讨论A所占体积分数如何变化。
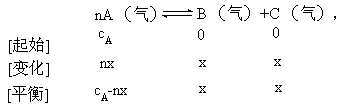
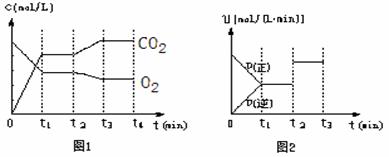
由于A所占体积分数受到两方面的制约,即A的大小(cA-nx)和总体积的大小(cA-nx+2x),而这两个量都是变量,因此其比值如何变化难以确定。另一方面反应物只有一种物质,增加其量是从增大浓度分析还是从加大压强考虑。知识的缺陷和分析方法的不当,往往得出以上各种错误的选择。
本题一种![]() 简捷思考方法是:当A的量增大一倍时,先将容器的体积也扩大一倍(其状况和第一次完全相同),这样达到平衡时,A所占体积分数不变。然后再将体积压缩到原状态,这时根据反应前后的气体体积数如何变化,考虑平衡如何移动,决定A所占体积分数如何变化。如当本题反应物A前的系数n等于1,由于反应前气体的总体积数小于反应后气体的总体积数,因此在压缩到原状态时,
简捷思考方法是:当A的量增大一倍时,先将容器的体积也扩大一倍(其状况和第一次完全相同),这样达到平衡时,A所占体积分数不变。然后再将体积压缩到原状态,这时根据反应前后的气体体积数如何变化,考虑平衡如何移动,决定A所占体积分数如何变化。如当本题反应物A前的系数n等于1,由于反应前气体的总体积数小于反应后气体的总体积数,因此在压缩到原状态时,
![]()
大,A所占体积分数增大,即N>M。若n等于3,由于反应前气体的总体积数大于反应后气体的总体积数,因此在压缩到原状态时,平衡将
![]()
减少,A所占体积分数减小,其结果为M>N。若n等于2,在压缩到原状态时,平衡不移动,其结果为M=N。
【状元纠错】由于A所占体积分数受到两方面的制约,即A的大小和总体积的大小,而这两个量都是变量,其比值如何变化难以确定。


 ,
, ,所以
,所以