氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉电池,氢镍电池的总反应式是![]() H2+NiO(OH)
H2+NiO(OH)![]() Ni(OH)2( )
Ni(OH)2( )
A.电池放电时,电池负极周围溶液pH不断增大
B.电池放电时,镍元素被氧化
C.电池放电时,氢元素被还原
D.电池放电时,H2是负极
解析:氢镍电池总反应为![]() H2+NiO(OH)
H2+NiO(OH)![]() Ni(OH)2据此,可列出正负极的半反应,负极H2+OH-→H2O+e-,正极:NiO(OH)+H2O+e-→Ni(OH)2+OH-依照两个电池半反应对各选项进行判断。选项A从负极反应式可以看出,放电时负极因OH-离子的介入而消耗。因此,周围溶液的H+浓度增在,pH变小而不是增大。从正极半反应可见,NiO(OH)中的Ni由+3价变成Ni(OH)2中+2价的Ni,应是被还原了,而不是被氧化,选项B也不正确,从负极半反应式来看,当放电时;H2中的H(0价)变为+1价,由此氢元素被氧化,选项C错,故D项正确。
Ni(OH)2据此,可列出正负极的半反应,负极H2+OH-→H2O+e-,正极:NiO(OH)+H2O+e-→Ni(OH)2+OH-依照两个电池半反应对各选项进行判断。选项A从负极反应式可以看出,放电时负极因OH-离子的介入而消耗。因此,周围溶液的H+浓度增在,pH变小而不是增大。从正极半反应可见,NiO(OH)中的Ni由+3价变成Ni(OH)2中+2价的Ni,应是被还原了,而不是被氧化,选项B也不正确,从负极半反应式来看,当放电时;H2中的H(0价)变为+1价,由此氢元素被氧化,选项C错,故D项正确。
答案:D
关于如图装置的叙述中,正确的是( )
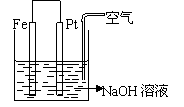
A.这是电解NaOH溶液的装置
B.这是一个原电池装置
C.Pt为正极,其电极反应为2H++2e-→H2↑
D.Fe为负极,其电极反应为4OH-→2H2O+O2↑+4e-
B
阿波罗宇宙飞船上使用的是氢氧燃电池,其电池总反应式为:2H2+O2=2H2O,电解液为KOH溶液,反应保持在较高温度使水蒸发,下列叙述中正确的是( )
A.此电池能见到淡蓝色火焰
B.H2为正极,O2为负极
C.工作时,电解液的pH不断减小
D
锌锰干电池在放电时,电池总反应方程式,可以表示为Zn(s)+2MnO2+2NH4+=Zn2++Mn2O3(s)+2NH3+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
A.Zn B.碳 C.MnO2和NH4+ D.Zn2+和NH3
C
燃料电池具有能量转化交率高等优点,具有很好的发展前景。有一种燃料电池,用石墨做电极,电解质溶液是KOH溶液,在两极上分别通入乙烷气体和氧气。请写出电极反应和电池总反应。
负极:C2H6+18OH-→2CO32-+12H2O+14e-
正极:O2+2H2O+4e-→4OH- 电池反应:2C2H6+702+8OH-=4CO32-+10H2O
本卷还有8题,登录并加入会员即可免费使用哦~

该作品由: 用户小小分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。