为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。以下说法不正确的是
ZnO(s)+2Ni(OH)2(s)。以下说法不正确的是
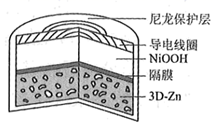
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.充电时阳极反应为Ni(OH)2(s)+OH−(aq)−e−![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C.放电时负极反应为Zn(s)+2OH−(aq)−2e−![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D.放电过程中OH−通过隔膜从负极区移向正极区
D
【详解】
A、三维多孔海绵状Zn具有较高的表面积,吸附能力强,所沉积的ZnO分散度高,A正确;
B、充电相当于是电解池,阳极发生失去电子的氧化反应,根据总反应式可知阳极是Ni(OH)2失去电子转化为NiOOH,电极反应式为Ni(OH)2(s)+OH-(aq)-e-=NiOOH(s)+H2O(l),B正确;
C、放电时相当于是原电池,负极发生失去电子的氧化反应,根据总反应式可知负极反应式为Zn(s)+2OH-(aq)-2e-=ZnO(s)+H2O(l),C正确;
D、原电池中阳离子向正极移动,阴离子向负极移动,则放电过程中OH-通过隔膜从正极区移向负极区,D错误。
答案选D。
我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是
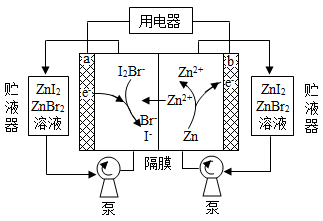
A.放电时,a电极反应为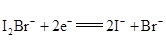
B.放电时,溶液中离子的数目增大
C.充电时,b电极每增重![]() ,溶液中有
,溶液中有![]() 被氧化
被氧化
D.充电时,a电极接外电源负极
D
【分析】
放电时,Zn是负极,负极反应式为Zn-2e-═Zn2+,正极反应式为I2Br-+2e-=2I-+Br-,充电时,阳极反应式为Br-+2I--2e-=I2Br-、阴极反应式为Zn2++2e-=Zn,只有阳离子能穿过交换膜,阴离子不能穿过交换膜,据此分析解答。
【详解】
A、放电时,a电极为正极,碘得电子变成碘离子,正极反应式为I2Br-+2e-=2I-+Br-,故A正确;
B、放电时,正极反应式为I2Br-+2e-=2I-+Br-,溶液中离子数目增大,故B正确;
C、充电时,b电极反应式为Zn2++2e-=Zn,每增加0.65g,转移0.02mol电子,阳极反应式为Br-+2I--2e-=I2Br-,有0.02molI-失电子被氧化,故C正确;
D、充电时,a是阳极,应与外电源的正极相连,故D错误;
故选D。
【点睛】
本题考查化学电源新型电池,会根据电极上发生的反应判断正负极是解本题关键,会正确书写电极反应式,易错选项是B,正极反应式为I2Br-+2e-=2I-+Br-,溶液中离子数目增大。
用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为![]() 混合溶液。下列叙述错误的是
混合溶液。下列叙述错误的是
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为:![]()
D.硫酸根离子在电解过程中向阳极移动
C
【解析】
A、根据原理可知,Al要形成氧化膜,化合价升高失电子,因此铝为阳极,故A说法正确;B、不锈钢网接触面积大,能增加电解效率,故B说法正确;C、阴极应为阳离子得电子,根据离子放电顺序应是H+放电,即2H++2e-=H2↑,故C说法错误;D、根据电解原理,电解时,阴离子移向阳极,故D说法正确。
锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O===2Zn(OH)42-。下列说法正确的是( )
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-) 逐渐减小
C.放电时,负极反应为:Zn+4OH–-2e–= Zn(OH)42-
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
C
【详解】
A.充电时,阳离子向阴极移动,即K+向阴极移动,A项错误;
B.放电时总反应为2Zn+O2+4OH–+ 2H2O=2Zn(OH)42-,则充电时生成氢氧化钾,溶液中的氢氧根离子浓度增大,B项错误;
C.放电时,锌在负极失去电子,电极反应为Zn+4OH–-2e–=Zn(OH)42-,C项正确;
D.标准状况下22.4L氧气的物质的量为1摩尔,电路中转移4摩尔电子,D项错误;
答案选C。
【点睛】
电极反应式的书写是电化学中必考的一项内容,一般先写出还原剂(氧化剂)和氧化产物(还原产物),然后标出电子转移的数目,最后根据原子守恒和电荷守恒完成缺项部分和配平反应方程式,作为原电池,正极反应式为:O2+2H2O+4e-=4OH-,负极电极反应式为:Zn+4OH–-2e–=Zn(OH)42-;充电是电解池,阳离子在阴极上放电,阴离子在阳极上放电,即阳离子向阴极移动,阴离子向阳极移动,对可充电池来说,充电时原电池的正极接电源正极,原电池的负极接电源的负极,不能接反,否则发生危险或电极互换,电极反应式是原电池电极反应式的逆过程;涉及到气体体积,首先看一下有没有标准状况,如果有,进行计算,如果没有必然是错误选项。
科学家近年发明了一种新型Zn−CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
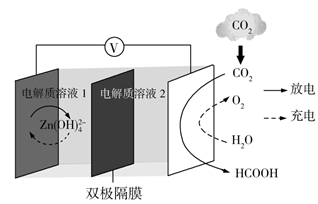
下列说法错误的是
A.放电时,负极反应为![]()
B.放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为![]()
D.充电时,正极溶液中OH−浓度升高
D
【分析】
由题可知,放电时,CO2转化为HCOOH,即CO2发生还原反应,故放电时右侧电极为正极,左侧电极为负极,Zn发生氧化反应生成![]() ;充电时,右侧为阳极,H2O发生氧化反应生成O2,左侧为阴极,
;充电时,右侧为阳极,H2O发生氧化反应生成O2,左侧为阴极,![]() 发生还原反应生成Zn,以此分析解答。
发生还原反应生成Zn,以此分析解答。
【详解】
A.放电时,负极上Zn发生氧化反应,电极反应式为:![]() ,故A正确,不选;
,故A正确,不选;
B.放电时,CO2转化为HCOOH,C元素化合价降低2,则1molCO2转化为HCOOH时,转移电子数为2mol,故B正确,不选;
C.充电时,阳极上H2O转化为O2,负极上![]() 转化为Zn,电池总反应为:
转化为Zn,电池总反应为:![]() ,故C正确,不选;
,故C正确,不选;
D.充电时,正极即为阳极,电极反应式为:![]() ,溶液中H+浓度增大,溶液中c(H+)•c(OH-)=KW,温度不变时,KW不变,因此溶液中OH-浓度降低,故D错误,符合题意;
,溶液中H+浓度增大,溶液中c(H+)•c(OH-)=KW,温度不变时,KW不变,因此溶液中OH-浓度降低,故D错误,符合题意;
答案选D。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户huan分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。