设NA表示阿伏加德罗常数,下列说法正确的是
A. 常温常压下,28 g CO和N2的混合气体一定含有2NA个原子
B. 1 L 0.1 mol/L NaHSO4溶液中含有0.1 NA个HSO4-
C. 将0.1 mol FeCl3溶于沸水制成胶体,其中含有的胶体粒子数目为0.1 NA
D. 0.2mol/L KCl溶液中含有0.2 NA个Cl-
【答案】A
【解析】
【详解】A. CO和N2的相对分子质量均为28,均为双原子分子,所以28 g CO和N2的混合气体的物质的量为1mol,含有的原子总数一定为2NA,故A正确;
B.硫酸氢钠在溶液中完全电离,硫酸氢钠溶液中不存在硫酸氢根离子,故B错误;
C. 因为氢氧化铁胶体中,氢氧化铁胶粒为氢氧化铁的聚集体,将0.1 mol FeCl3溶于沸水制成胶体,其中含有的胶体粒子数目小于0.1 NA,故C错误;
D. 没有给定溶液的体积,无法计算出0.2mol/LKCl溶液中含有Cl-的数目,故D错误;
综上所述,本题选A。
【点睛】硫酸氢钠属于强酸的酸式盐,在水溶液中完全电离出三种离子:NaHSO4=Na++H++SO42-;在熔融的条件下,电离出2种离子:NaHSO4=Na++HSO4-。
有 Na2SO4和 Fe2(SO4)3的混合液,已知其中 Fe3+的物质的量浓度为 0.4 mol/L,SO42-的物质的量浓度为 0.7 mol/L,则此溶液中 Na+的物质的量浓度为
A. 0.1 mol/L B. 0.15 mol/L C. 0.2 mol/L D. 0.25 mol/L
【答案】C
【解析】
试题分析:根据溶液中的电荷守恒有:c(Na+) +3 c(Fe3+)="2" c(SO42-) ,有c(Na+) +3×0.4 mol/L="0.7" mol/L×2
c(Na+)=0.2 mol/L
考点:电荷守恒的运用。
如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
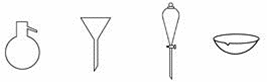
A. 蒸馏、蒸发、萃取、过滤 B. 过滤、蒸发、萃取、蒸馏
C. 萃取、过滤、蒸馏、蒸发 D. 蒸馏、过滤、萃取、蒸发
【答案】D
【解析】
【分析】
根据化学实验基础操作及注意事项分析。
【详解】图中给定的仪器:蒸馏烧瓶(蒸馏)、普通漏斗(过滤)、分液漏斗(分液或萃取)、蒸发皿(蒸发),故D正确。
故选D。
【点睛】带支管口的是蒸馏烧瓶,不带支管的是圆底烧瓶。
用NA表示阿伏加德罗常数,下列叙述不正确的是
A. 25 ℃、1.01×105 Pa时,44 g CO2中含有的氧原子数为2NA
B. 3.2g由O2和O3组成的混合物中含有的原子数目为0.2NA
C. 在过氧化钠与水的反应中,每消耗0.1mol过氧化钠,转移电子的数目为0.1NA
D. 在KClO3+6HCl(浓) ===KCl+3Cl2↑+3H2O反应中,若产生标准状况下6.72LCl2时,转移电子数目为0.6NA
【答案】D
【解析】
【详解】A、44g二氧化碳的物质的量为1mol,而二氧化碳中含2个氧原子,故1mol二氧化碳中含2NA个氧原子,选项A正确;
B、氧气和臭氧均由氧原子构成,故3.2g混合物中含有的氧原子的物质的量为0.2mol,个数为0.2NA个,选项B正确;
C、Na2O2与H2O的反应为歧化反应:2Na2O2+2H2O=4NaOH+O2↑,此反应转移2mol电子,生成1molO2,故当每消耗0.1mol过氧化钠,转移电子的物质的量为0.1mol,数目为0.1NA,选项C正确;
D.在KClO3+6HCl(浓) =KCl+3Cl2↑+3H2O反应中,根据化合价升降可以判断,每生成3molCl2转移5mol电子,标准状况下6.72LCl2的物质的量为![]() =0.3mol,则转移电子物质的量为0.5mol,数目为0.5NA,选项D不正确;
=0.3mol,则转移电子物质的量为0.5mol,数目为0.5NA,选项D不正确;
答案选D。
“钴酞菁”分子(直径约为1.34x10-9m)结构和性质与人体内的血红素及植物内的叶绿素非常相似。下列关于“钴酞菁”分子的说法中正确的是
A. “钴酞菁”分子在水中所形成的分散系属悬浊液
B. “钴酞菁”分子既能透过滤纸,也能透过半透膜
C. 在分散系中,“钴酞菁”分子直径比Na+的直径小
D. “钴酞菁”分子在水中形成的分散系能产生丁达尔现象
【答案】D
【解析】
试题分析:由于“钴酞菁”分子(直径约为1.34×10-9m),所以“钴酞菁”分子在水中所形成的分散系属于胶体,选项D正确,A不正确。胶体粒子不能通过半透膜,B不正确。在分散系中,“钴酞菁”分子直径比Na+的直径大,C不正确,答案选D。
考点:考查胶体的性质以及三种分散系的区别
点评::该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确三种分散系的本质区别。
本卷还有18题,登录并加入会员即可免费使用哦~

该作品由: 用户白杨分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。