【化学——选修5:有机化学基础】(15分)
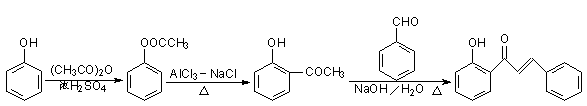
华法林(Warfarin)又名杀鼠灵,想美国食品药品监督管理局批准为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称为 ,E中官能团名称为 。
(2)B的结构简式为 。
(3)由C生成D的化学方程式为 。
(4)⑤的反应类型为 ,⑧的反应类型为 。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有 种。
a.能与FeCl3溶液发生显色反应 b.能发生银镜反应
其中核磁共振氢谱为五组峰的结构简式为 。
(6)参照上述合成路线,设计一条由苯酚(![]() )、乙酸酐(CH3CO)2O和苯甲醛(
)、乙酸酐(CH3CO)2O和苯甲醛(![]() )为原料,制备
)为原料,制备![]() 的合成路线(其他无机试剂任选)。
的合成路线(其他无机试剂任选)。
1)甲苯(1 分) 酯基(1 分)(2)![]() (2 分)
(2 分)
(3)![]() (2 分)(反应物和生成物书写正确得 1 分,配平、“→”、反应条件均正确得 1 分)
(2 分)(反应物和生成物书写正确得 1 分,配平、“→”、反应条件均正确得 1 分)
(4)取代反应(1 分) 加成反应(1 分)
(5)13(2 分) ![]() (2 分)
(2 分)
(6)(3 分)(每 1 步 1 分)
【化学——选修3:物质结构与性质】(15分)
以铁矿石(Fe2O3)为起始物,经过一系列反应可以得到Fe3[Fe(CN)6]2和Fe(SCN)3,请回答下列问题:
(1)写出Fe的原子结构示意图 ,O原子核外电子轨道表示式为 。
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为 。SCN-的空间构型
(3)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为 ,该化学键能够形成的原因是 。
 (4)K3[Fe(CN)5NO]的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是_ ,该配合物中铁原子的配位数是 。
(4)K3[Fe(CN)5NO]的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是_ ,该配合物中铁原子的配位数是 。
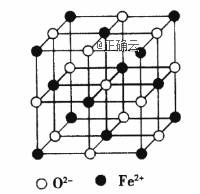
(5)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为 ,若该晶胞边长为anm,
则该晶体密度为 g·cm-3(阿伏伽德罗常数的值为NA)。
(15分)(1)![]() (1分)
(1分) ![]() (2分)
(2分)
(2)CO2、N2O、CS2、COS等(1分,任写一种即可) 直线形(2分)
(3)配位键(1分)CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道)(2分) (4)C<O<N(1分) 6(1分)
(5)6(2分) ![]() g/cm3 (2分)
g/cm3 (2分)
 某化学工厂产生的酸洗废液中含有Fe3+、Ni2+、NO3-、F-和Cr2O72-等离子。综合利用该酸洗废液的工艺流程如下:
某化学工厂产生的酸洗废液中含有Fe3+、Ni2+、NO3-、F-和Cr2O72-等离子。综合利用该酸洗废液的工艺流程如下:
已知:①Ni2+与足量氨水的反应为:Ni2++6NH3 ![]() [Ni(NH3)6]2+
[Ni(NH3)6]2+
②金属离子开始沉淀和沉淀完全时的pH如右表 ③Ksp(CaF2)=4x10-11
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
回答下列问题:
(1)再生酸中主要含有硝酸,采取减压蒸馏的原因是
(2)渣1的主要成份为 (填化学式)
(3)转化时发生反应的离子方程式
(4)用平衡移动的原理解释沉镍的原理
(5)渣3的主要成分为氢氧化钙和 、 (填化学式)
(6)国家排放标准要求c(F-)≤3.8 mg•L-1。残液中残留的Ca2+浓度至少应为 mg•L-1
(1) 降低蒸馏温度,以减少硝酸的分解 (2)Fe(0H)3
(3) 5H++Cr2O72﹣+3HSO3﹣=2Cr3++3SO42﹣+4H2O
(4)Ni3++6NH3![]() [Ni(NH3)6]加入S2-与Ni3+结合生成沉淀,促使上述平衡逆向移动
[Ni(NH3)6]加入S2-与Ni3+结合生成沉淀,促使上述平衡逆向移动
(5)CaSO4、CaF2 (6)40
燃煤烟气的脱硫脱硝是目前研究的热点。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
 ①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ•mol-1
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ•mol-1
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H= -1160 kJ•mol-1
③H2O(g) = H2O(l) △H= -44 kJ•mol-1
则CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(l) △H= kJ/mol
(2)某科研小组研究臭氧氧化--碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+ O3(g) ![]() NO2(g)+O2(g) △H1 = -200.9 kJ•mol-1 Ea1 = 3.2 kJ•mol-1
NO2(g)+O2(g) △H1 = -200.9 kJ•mol-1 Ea1 = 3.2 kJ•mol-1
反应Ⅱ:SO2(g)+ O3(g) ![]() SO3(g)+O2(g) △H2 = -241.6 kJ•mol-1 Ea2 = 58 kJ•mol-1
SO3(g)+O2(g) △H2 = -241.6 kJ•mol-1 Ea2 = 58 kJ•mol-1
已知该体系中臭氧发生分解反应:2O3(g) ![]() 3O2(g)。请回答:
3O2(g)。请回答:
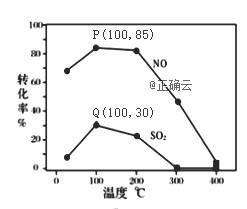
其它条件不变,每次向容积为2L的反应器中充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0 mol O3,改变温度,反应相同 时间t后体系中NO和SO2的转化率如图所示:
①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因 。
②下列说法正确的是 。
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
③假设100℃时P、Q均为平衡点,此时反应时间为10分钟,发生分解反应的臭氧占充入臭氧总量的10%,NO的平均反应速率为 ;反应Ⅱ在此时的平衡常数为 。
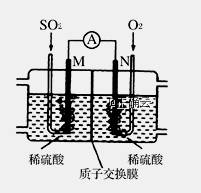
(3)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
①M极发生的电极反应式为 。
②当外电路通过0.2 mol电子时,质子交换膜左侧的溶液质量 (填“增大”或“减小”)、 克。
(1)-955 (2分)
(2)①反应Ⅰ的活化能小于反应Ⅱ,相同条件下更易发生反应 (2分) ②BC (2分)
③ 0.0425mol/(L·min) (2分) 0.96 (2分)
(3)①SO2+2H2O-2e- =SO42- +4H+(2分) ②增大 (1分)6.2(2分)
亚氯酸钠(NaClO2)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出ClO2,ClO2有类似Cl2的性质。某兴趣小组探究亚氯酸钠的制备与性质。
Ⅰ.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量ClO2,充分反应。
(1)仪器a的名称为______________,仪器b的作用是______________。
(2)装置A中生成NaClO2的离子方程式为____________________________。
(3)若从装置A反应后的溶液中获得NaClO2晶体,则主要操作有减压蒸发浓缩、
、 、洗涤、干燥等。
Ⅱ.探究亚氯酸钠的性质
停止通ClO2气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
(4)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因 。
(5)B中现象为 。产生该现象的离子方程式为 。
(6)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①, 。
(14分)(1)烧瓶(圆底烧瓶)(1分) 防止倒吸(1分)
(2)2ClO2+2OH-+H2O2=2ClO2-+H2O+O2↑(2分,凡是反应物或生成物有误均不得分,配平错误扣 1 分,漏写“↑”不扣分)
(3)降温结晶(1分) 过滤 (1分)
(4)NaClO2与H2SO4反应生成的Cl-对反应起催化作用(2分,NaCl或反应产物有催化作用也得分)
(5)溶液变蓝色(2分) 2ClO2+10I-+8H+=2Cl-+5I2+4H2O (2分)
(6)从进气口通入一段时间的空气(2分)
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户公牛分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。