海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示),下列有关说法正确的是( )
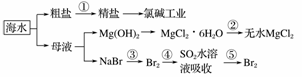
A.第①步除去粗盐中的SO![]() 、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.第②步结晶出的MgCl2·6H2O可在HCl气流中加热分解制无水MgCl2
C.在第③④⑤步中溴元素均被氧化
D.第⑤步涉及的分离操作有过滤、萃取、蒸馏
答案 B
解析 选项中的试剂添加顺序中,钡离子最后无法除去,则加入的药品顺序为BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故A错误;步骤②中的MgCl2·6H2O在脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解,故MgCl2·6H2O可在HCl氛围中加热脱水制得无水MgCl2,故B正确;第③步将溴离子氧化为溴单质,第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质,故C错误;第⑤步中,溴元素化合价从-1升高到0价,被氧化,生成的单质溴溶于水,则萃取分液后蒸馏即可分离,不需要过滤操作,故D错误。
工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法不正确的是( )

A.在铝土矿制备较高纯度Al的过程中常用到NaOH溶液、CO2气体、冰晶石
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C.在制粗硅时,被氧化的物质与被还原的物质的物质的量之比为2∶1
D.黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
答案 B
解析 用铝土矿制备较高纯度Al,首先用NaOH溶液将铝土矿中的氧化铝溶解转化为偏铝酸钠溶液,然后过滤、向滤液中通入CO2气体把偏铝酸钠转化为氢氧化铝沉淀,再过滤得氢氧化铝,接着加热氢氧化铝让其分解为氧化铝,最后用冰晶石作助熔剂,电解熔融的氧化铝得到铝,所以A正确;石英的主要成分是二氧化硅,它属于酸性氧化物不与盐酸反应,玻璃的主要成分有二氧化硅、硅酸钠、硅酸钙,组成中有盐故被称为硅酸盐产品,它也不能与盐酸反应,实验室经常用玻璃瓶盛放盐酸,所以B不正确;在制粗硅时,发生反应SiO2+2C![]() Si+2CO↑,被氧化的物质C与被还原的物质SiO2的物质的量之比为2∶1,C正确;黄铜矿(CuFeS2)与O2反应,铜由+2价降为+1价被还原得到Cu2S、氧由0价降至-2价得到FeO,所以Cu2S、FeO均是还原产物,D正确。
Si+2CO↑,被氧化的物质C与被还原的物质SiO2的物质的量之比为2∶1,C正确;黄铜矿(CuFeS2)与O2反应,铜由+2价降为+1价被还原得到Cu2S、氧由0价降至-2价得到FeO,所以Cu2S、FeO均是还原产物,D正确。
溴化钙是一种重要的化工原料,制备CaBr2·2H2O 的主要流程如下:
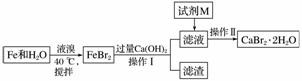
下列说法不正确的是( )
A.试剂M 是HBr,加入HBr的目的是除去过量的Ca(OH)2
B.操作Ⅰ为过滤,滤渣为Fe、Fe(OH)2和Fe(OH)3;操作Ⅱ为重结晶,具体操作步骤为蒸发浓缩、冷却结晶、洗涤、干燥
C.制得的CaBr2·2H2O 可以通过以下方法测定纯度:称取一定量的样品溶于水,滴入足量Na2CO3 溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却、称量,计算便得出CaBr2·2H2O的纯度
D.工业上也可以将氨气通入石灰乳,并加入溴,于65 ℃进行反应,制得溴化钙,此反应中还会生成一种无色气体,该反应的化学方程式为3Ca(OH)2+3Br2+2NH3![]() 3CaBr2+N2+6H2O
3CaBr2+N2+6H2O
答案 B
解析 Fe与溴单质反应生成FeBr2 ,加过量的氢氧化钙,生成氢氧化亚铁沉淀,氢氧化亚铁易被氧气氧化为氢氧化铁,过滤得到滤液中主要含有CaBr2 ,在滤液中加HBr中和多余的氢氧化钙,然后蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到CaBr2·2H2O晶体。根据上述分析,溴化亚铁溶液中加入过量的氢氧化钙,过滤得到的滤液含有溴化钙和氢氧化钙,加溴化氢除去多余的氢氧化钙,则加入的M为HBr,故A正确;氢氧化亚铁易被氧气氧化为氢氧化铁,操作Ⅰ为过滤,滤渣为Fe和Fe(OH)3,故B错误; 称取一定量的样品溶于水,滴入足量Na2CO3 溶液,充分反应后过滤得到生成的碳酸钙沉淀,将滤渣洗涤、烘干、冷却、称量氧化钙的质量,可以得出CaBr2·2H2O的纯度,故C正确;3Ca(OH)2+3Br2+2NH3![]() 3CaBr2+N2+6H2O,因此工业上也可以将氨气通入石灰乳,并加入溴,于65 ℃进行反应,制得溴化钙,故D正确。
3CaBr2+N2+6H2O,因此工业上也可以将氨气通入石灰乳,并加入溴,于65 ℃进行反应,制得溴化钙,故D正确。
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌,以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③HClO2可看成是强酸。
则下列说法不正确的是( )
A.在发生器中鼓入空气的作用可能是稀释ClO2以防止爆炸
B.吸收塔内发生反应的离子方程式:2ClO2+H2O2—→2HClO2+O2
C.吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中,除H2O2外,还可以选择还原性适中的Na2O2
D.从滤液中得到的NaClO2·3H2O为粗晶体,要得到更加纯净的NaClO2·3H2O晶体必须进行重结晶操作
答案 B
解析 根据题中所给信息,ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下,因此发生器中鼓入空气的作用是稀释ClO2防止爆炸,故A说法正确;根据流程,吸收塔内发生的离子方程式为2OH-+H2O2+2ClO2===2ClO![]() +2H2O+O2↑,故B说法错误;H2O2和Na2O2都含有过氧键,故C说法正确;粗晶体提纯,需要进行重结晶,故D说法正确。
+2H2O+O2↑,故B说法错误;H2O2和Na2O2都含有过氧键,故C说法正确;粗晶体提纯,需要进行重结晶,故D说法正确。
为了从海带浸取液中提取碘,某同学设计了如下实验方案:
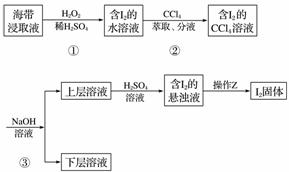
下列说法正确的是( )
A.①中反应的离子方程式:2I-+ H2O2=== I2+ 2OH-
B.②中分液时含I2的CCl4溶液从分液漏斗上口倒出
C.③中得到的上层溶液中含有I-
D.操作Z的名称是加热
答案 C
解析 ①中在酸性溶液中不可能生成OH-,故A错误;四氯化碳的密度比水大,②中分液时含I2的CCl4溶液从分液漏斗下口放出,故B错误;碘化钠水溶液的密度比四氯化碳小,③中得到的上层溶液中含有I-,故C正确;从含有碘的悬浊液中得到碘,应该采用过滤的方法,故D错误。
本卷还有3题,登录并加入会员即可免费使用哦~

该作品由: 用户闵婕分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。