化学充实、改变了生活,与工农业生产,科技发展等密切相关。下列相关说法正确的是
A. 因为NaHCO3能与酸反应,所以患有胃溃疡的病人在胃酸过多时可以服用含NaHCO3的药片
B. 四氯化碳曾用作灭火剂,但因与水高温下反应时会产生有毒物质,现已禁用
C. 石油的催化裂解是为了提高从石油中得到汽油等轻质液体燃料的产量
D. 石墨烯是由碳原子紧密排列而成的具有多层三维蜂窝状的碳材料,层内碳原子位于正六角形的角顶点
【答案】B
【解析】分析:A.小苏打产气过多,会发生溃疡穿孔;B.因为四氯化碳在500℃以上时,可以与水作用,产生有毒的光气(COCl2)和盐酸(HCl),所以禁用;C.石油的催化裂解是使具有长链的烃深度裂化断裂成各种短链的气态不饱和烃和少量液态烃;D.石墨烯是一种二维晶体,人们常见的石墨是由一层层以蜂窝状有序排列的平面碳原子堆叠而形成的,石墨的层间作用力较弱,很容易互相剥离,形成薄薄的石墨片,当把石墨片剥成单层之后,这种只有一个碳原子厚度的单层就是石墨烯。
详解:A.小苏打产气过多,会发生溃疡穿孔,A错误;B、CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒的光气(COCl2)和盐酸(HCl),现已被禁用,B正确;C.石油的催化裂解是使具有长链的烃深度裂化断裂成各种短链的气态不饱和烃和少量液态烃,C错误;D.石墨烯是一种二维晶体,只有一个碳原子厚度的单层结构,D错误;因此,本题答案为B。
点睛:裂化和裂解不同,裂化是为了提高从石油中得到汽油等轻质液体燃料的产量,而裂解是使具有长链的烃深度裂化断裂成各种短链的气态不饱和烃和少量液态烃;石墨和石墨烯的区别:石墨是由一层层以蜂窝状有序排列的平面碳原子堆叠而形成的,石墨的层间作用力较弱,很容易互相剥离,形成薄薄的石墨片,当把石墨片剥成单层之后,这种只有一个碳原子厚度的单层就是石墨烯。
下列实验装置不能达到实验目的的是
| A | B | C | D |
|
|
|
|
|
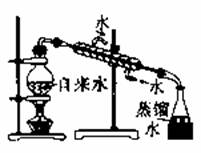
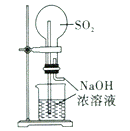
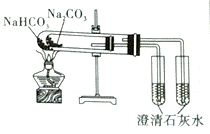
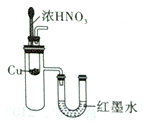
| 实验室制取蒸馏水 | 用SO2和NaOH溶液做喷泉实验 | 证明Na2CO3 的热稳定性比NaHCO3好 | 证明铜与浓硝酸的反应是放热反应 |
A. A B. B C. C D. D
【答案】C
【解析】分析:A.依据制取蒸馏水原理分析;B.根据产生喷泉的原理分析;C.依据碳酸氢钠分解温度分析;D.根据实验现象判断。
详解:A.符合制取蒸馏水的原理,A正确;
B.二氧化硫易溶于氢氧化钠溶液,使烧瓶中气体压强减小,烧杯中的液体进入烧瓶,产生喷泉,B正确;
C项,装置中两者受热温度不同,但是碳酸氢钠在较低温度下就能分解而碳酸钠在较高温度下不分解,因此不能说明碳酸钠比碳酸氢钠稳定,故C错误;
D.若为放热反应,则试管中气体受热,压强增大,U形管中液面,左边下降,右边上升,故D正确;综上所述,本题答案为C。
下列说法正确的是
A. 往明矾溶液中加入氢氧化钡溶液至沉淀质量最大时,离子反应的方程式为:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
B. 在反H2S+H2SO4(浓)=S↓+SO2+2H2O中, 转移电子的数目是2NA
C. 由于AgCl的Ksp为1.8×10-10,而Ag2CrO4的Ksp为1.9×10-12(前者比后者大),所以往浓度均为0.001mol/L的NaCl、K2CrO4混合溶液中滴加AgNO3溶液,先生成Ag2CrO4沉淀
D. 在同时加有 3mol Na3PO4、2molNaH2PO4的水溶液中存在如下恒等关系: 2c(PO43-)=3c(H2PO4-)
【答案】A
【解析】分析:A.由于硫酸钡的摩尔质量比氢氧化铝的摩尔质量大,生成硫酸钡最多时,沉淀质量最大;B.计算转移电子数需要知道参加反应的物质的量,否则无法计算;C. AgCl和 Ag2CrO4类型不同,不能直接通过Ksp大小比较沉淀先后;D. Na3PO4和NaH2PO4在溶液中存在水解和电离等平衡关系,以此解答。
详解:A.由于硫酸钡的摩尔质量比氢氧化铝的摩尔质量大,生成硫酸钡最多时,沉淀质量最大,此时氢氧化铝恰好全部溶解,离子方程式Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
故A正确;
B.计算转移电子数需要知道参加反应的物质的量,否则无法计算,故B错误;
C. AgCl的Ksp为1.8×10-10,Ag2CrO4的Ksp为1.9×10-12,沉淀0.001mol/L的Cl-,需要Ag+,c(Ag+)=![]() mol/L=1.8×10-7mol/L, 沉淀0.001mol/L的CrO42-,需要Ag+,c(Ag+)=
mol/L=1.8×10-7mol/L, 沉淀0.001mol/L的CrO42-,需要Ag+,c(Ag+)=![]() mol/L=1.9×10-6mol/L, 所以先生成AgCl沉淀,C错误;
mol/L=1.9×10-6mol/L, 所以先生成AgCl沉淀,C错误;
D. Na3PO4和NaH2PO4由于水解和电离c(PO43-)和c(H2PO4-)发生变化,不再有2c(PO43-)=3c(H2PO4-)的关系,故D错误;所以本题正确答案为:A。
点睛:本题A选项,不要将生成沉淀质量最大和生成沉淀物质的量最大相混淆,若要生成沉淀的物质的量最大,则硫酸钡和氢氧化铝同时生成,此时离子方程式为:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓。
设NA表示阿伏加德罗常数的值,下列说法错误的有
①17.6 g丙烷中所含的共价健数为4 NA
②常温下,21 g C3H6和C4H8的混合物中含有的碳原子数为1.5 NA
③电解硫酸铜溶液,往电解后的溶液中加入氧化铜一定可以使溶液恢复到原来的状态
④2g D216O中含有的质子数、中子数、电子数均为NA
⑤1.0L、pH= 13的NaOH溶液中,OH-离子数目一定为0.1 NA
⑥将100mL、0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01 NA
A. 2项 B. 3项 C. 4项 D. 5项
【答案】B
【解析】分析: (1)丙烷分子中含有2个碳碳键、8个碳氢键,总共含有10个共价键;(2)丙烯与丁烯的最简式相同,均为CH2,根据最简式计算;(3) 电解硫酸铜溶液,若阴极无氢气产生,往电解后的溶液中加入氧化铜一定可以使溶液恢复到原来的状态,若有氢气产生,则不是;(4)D216O中含有质子数=核外电子数=2+8=10,中子数=(2-1)×2+(16-8)=10,质量数为4+16=20,所以2g D216O中含有的质子数、中子数、电子数均为1mol;
(5)未指明温度无法计算;(6) Fe(OH)3胶体粒子为氢氧化铁的聚集体。
详解:(1)丙烷的相对分子质量是44,所以17.6 g丙烷的物质的量是0.4 mol,因为每1 mol的该物质中含有共价键10 mol,所以0.4 mol中所含的极性共价键为4NA,故(1)正确;
(2)丙烯与丁烯的最简式相同,均为CH2,21 g C3H6和C4H8的混合物中含有的碳原子数为![]() =1.5NA,故(2)正确;
=1.5NA,故(2)正确;
(3) 若只电解电解硫酸铜溶液,阴极无氢气产生,往电解后的溶液中加入氧化铜一定可以使溶液恢复到原来的状态,若后期电解水,有氢气产生,则不能;故(3)错误;
(4) D216O中含有质子数=核外电子数=2+8=10,中子数=(2-1)×2+(16-8)=10,质量数为4+16=20,所以2g D216O中含有的质子数、中子数、电子数均为1mol,故(4)正确;
(5) 没有指明是常温,无法计算氢氧根离子浓度,故(5)错误;
(6) Fe(OH)3 胶体粒子为氢氧化铁的聚集体,无法计算胶体中含有的胶粒数目,故(6)错误;
③⑤⑥错误,所以本题选B。
点睛:用惰性电极电解硫酸铜溶液,开始时的反应为CuSO4+2H2O=Cu+H2SO4+O2↑(电解条件),此时从溶液中析出的是铜和氧气,相当于减少CuO,补充适量的CuO可以使溶液恢复到原来状态;若CuSO4不足,则继续电解水,此时减少的是水,需要加水恢复溶液。
用图所示装置电解硫酸铜和氯化钠的混合溶液,当线路中有1.20mol电子通过时,甲电极增重并有4.48L (已折算成标准状况下的体积,后同)气体生成,乙电极同时生成气体7.84L,则原溶液中硫酸铜与氯化钠的物质的量之比为
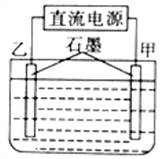
A. 2:1 B. 4:1 C. 2:3 D. 4:3
【答案】A
【解析】分析:本题考查电解原理,根据离子放电顺序,分析电极产物,根据电子守恒解答。
详解:该电解池可能发生的阴极反应为:①Cu2++2e-=Cu、②2H++2e-=H2↑;发生的阳极反应为:③2Cl--2e-=Cl2↑,④2H2O-4e-=4H++O2↑,甲电极增重,并有4.48L气体生成,则氢气体积为4.48L(标准状况),乙电极同时生成气体7.84L(氯气和氧气),反应共转移电子1.20mol,阴极反应中,反应②共得电子0.4mol电子,则反应①共得电子1.2mol-0.4mol=0.8mol,可计算得原溶液中含Cu2+,其物质的量为0.4mol;设阳极产生氯气物质的量为x,产生氧气物质的量为y,则x+y=![]() =0.35mol,共转移电子1.2mol,则2x+4y=1.2,联立两个方程,解得,x=0.1mol,y=0.25mol,所以溶液中含Cl-为0.2mol, 则原溶液中硫酸铜与氯化钠的物质的量之比为0.4:0.2=2:1,故选A项。综上所述,本题正确答案为A。
=0.35mol,共转移电子1.2mol,则2x+4y=1.2,联立两个方程,解得,x=0.1mol,y=0.25mol,所以溶液中含Cl-为0.2mol, 则原溶液中硫酸铜与氯化钠的物质的量之比为0.4:0.2=2:1,故选A项。综上所述,本题正确答案为A。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户yuanyuan分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。