下列有关说法不正确的是( )
| 选项 | A | B | C | D |
| 生活中的应用 |
月饼袋内放有小袋铁粉 |
口服补血剂(琥珀酸亚铁)并同时服维生C |
饼干包装盒内放有小袋硅胶 |
肉制品中添加适量的亚硝酸钠 |
| 作用 | 铁粉有抗氧化的作用 | 维生素C有防止Fe2+被还原的作用 | 硅胶有吸水的作用 | 亚硝酸钠有防腐的作用 |
A.A B.B C.C D.D
【考点】14:物质的组成、结构和性质的关系.
【分析】A.抗氧化的作用物质应具有还原性;
B.维生素C具有还原性;
C.依据硅胶的吸水性解答;
D.亚硝酸钠具有还原性.
【解答】解:A.铁粉具有还原性,能够防止食品氧化变质,故A正确;
B.维生素C有防止Fe2+被氧化的作用,故B错误;
C.硅胶具有吸水性,能够用于食品干燥剂,故C正确;
D.亚硝酸钠具有还原性,肉制品中添加适量的亚硝酸钠可以防止氧化变质,注意用量应在国家规定标准内,故D正确;
故选:B.
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用图表示. 下列关于海洋氮循环的说法正确的是( )
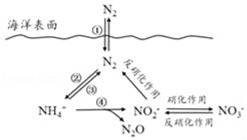

A.海洋中的氮循环起始于氮的氧化
B.海洋中的氮循环属于固氮作用的是③
C.海洋中的反硝化作用一定有氧气的参与
D.向海洋排放含NO3﹣的废水会影响海洋中NH4+的含量
【考点】EL:含氮物质的综合应用.
【分析】A.转化关系图可知海洋中的氮循环起始于氮的还原;
B.海洋中不存在游离态的氮,氮元素是以化合态存在;
C.反硝化作用是指将硝酸盐转变成氮气的过程.硝化作用是指氨在微生物作用下氧化为硝酸的过程.硝化细菌将氨氧化为硝酸的过程.反硝化作用:反硝化细菌在缺氧条件下,还原硝酸盐,释放出分子态氮(N2)或一氧化二氮(N2O)的过程;
D.转化关系图中硝酸根离子增多,反硝化作用增强;
【解答】解:A.转化关系图可知海洋中的氮循环起始于氮的还原,大气氮生成铵根离子,故A错误;
B.海洋中不存在游离态的氮,氮元素是以化合态存在,主要是硝酸根离子,故B错误;
C.反硝化作用是指将硝酸盐转变成氮气的过程.硝化作用是指氨在微生物作用下氧化为硝酸的过程.硝化细菌将氨氧化为硝酸的过程.反硝化作用:反硝化细菌在缺氧条件下,还原硝酸盐,释放出分子态氮(N2)或一氧化二氮(N2O)的过程,不一定有氧参加,故C错误;
D.转化关系图中硝酸根离子增多,反硝化作用增强,向海洋排放含NO3﹣的废水会影响海洋中NH4+的含量,故D正确;
故选D;
C和H2在生产、生活、科技中是重要的燃料.
①2C(s)+O2(g)═2CO(g)△H1=﹣220kJ/mol
②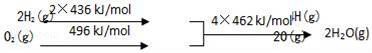

下列推断正确的是( )
A.C(s)的燃烧热110 kJ/mol
B.2H2(g)+O2(g)═2H2O(g)△H1=+480 kJ/mol
C.C(s)+H2O(g)═CO(g)+H2(g)△H1=+130 kJ/mol
D.欲分解2 mol H2O(l),至少需要提供4×462 kJ 的热量
【考点】BB:反应热和焓变.
【分析】A.燃烧热是指完全燃烧1mol物质生成最稳定产物的过程放出的热量;
B.水的结构式为H﹣O﹣H,2mol水分子中含有4molH﹣O键,2H2(g)+O2(g)═2H2O(g)△H=反应物总键能﹣生成物总键能,据此计算;
C.根据图示以及C(s)的燃烧热、氢气和氧气反应的热化学方程式构建目标方程式,结合盖斯定律进行计算;
D.根据2H2(g)+O2(g)═2H2O(g)△H=﹣480KJ/mol结合盖斯定律分析.
【解答】解:A.2C(s)+O2(g)═2CO(g)△H1=﹣220kJ/mol,C(s)+![]()
![]() O2(g)═CO(g)△H1=﹣110kJ/mol,但 C(s)的燃烧热指产物为稳定的二氧化碳所放出的热量,燃烧热大于110 kJ/mol,故A错误;
O2(g)═CO(g)△H1=﹣110kJ/mol,但 C(s)的燃烧热指产物为稳定的二氧化碳所放出的热量,燃烧热大于110 kJ/mol,故A错误;
B.水的结构式为H﹣O﹣H,2mol水分子中含有4molH﹣O键,2H2(g)+O2(g)═2H2O(g)△H=反应物总键能﹣生成物总键能=436kJ/mol×2+496kJ/mol﹣4×462kJ/mol=﹣480KJ/mol,故B错误;
C.①C(s)+![]()
![]() O2(g)═CO(g)△H1=﹣110kJ/mol,②2H2(g)+O2(g)═2H2O(g)△H=﹣480KJ/mol,由①﹣
O2(g)═CO(g)△H1=﹣110kJ/mol,②2H2(g)+O2(g)═2H2O(g)△H=﹣480KJ/mol,由①﹣![]()
![]() ×②得:C(s)+H2O(g)═CO(g)+H2(g)△H1=(﹣110kJ/mol)﹣
×②得:C(s)+H2O(g)═CO(g)+H2(g)△H1=(﹣110kJ/mol)﹣![]()
![]() ×(﹣480KJ/mol)=+130 kJ/mol,故C正确;
×(﹣480KJ/mol)=+130 kJ/mol,故C正确;
D.2H2(g)+O2(g)═2H2O(g)△H=﹣480KJ/mol,将方程式反应物和生成物颠倒,根据盖斯定律,则反应热变换符号,分解2 mol H2O(l),至少需要提供480KJ热量,故D错误;
故选C.
在浓碱作用下,苯甲醛自身可发生反应制备相应的苯甲酸 ( 在碱溶液中生成羧酸盐 ) 和苯甲醇,反应后静置,液体出现分层现象.有关物质的物理性质如表:下列说法不正确的是( )
| 苯甲醛 | 苯甲酸 | 苯甲醇 | |
| 沸点/℃ | 178.1 | 249.2 | 205.4 |
| 熔点/℃ | ﹣26 | 121.7 | ﹣15.3 |
| 溶解性 ( 常温 ) | 微溶于水,易溶于有机溶剂 | ||
A.苯甲醛既发生了氧化反应,又发生了还原反应
B.可用银氨溶液判断反应是否完全
C.反应后的溶液先用分液法分离出有机层,再用蒸馏法分离出苯甲醇
D.反应后的溶液中加酸、酸化后,用过滤法分离出苯甲酸
【考点】P3:蒸馏与分馏.
【分析】A.有机物化合物分子中增加氧原子或减少氢原子的反应称为氧化反应,增加氢原子或减少氧原子的反应称为还原反应;
B.醛基的特征反应是与银氨溶液发生银镜反应;
C.分离互不相容的液体的方法是分液,苯甲醛和苯甲醇的沸点相差较大;
D.苯甲酸易溶于有机溶剂.
【解答】解:A.苯甲醛→苯甲酸,增加了氧原子,属于氧化反应,苯甲醛→苯甲醇,增加了氢原子,属于还原反应,故A正确; B.苯甲醛含有醛基,能与银氨溶液发生银镜反应,因此可用银氨溶液判断反应是否完全,故B正确;C.反应后的溶液分为有机层和水层,互不相容,可用分液法分离,有几层中苯甲醛和苯甲醇的沸点相差较大,可用蒸馏法分离,故C正确;
D.反应后的溶液中加酸、酸化,苯甲酸进入有几层,应该分液后蒸馏,故D错误;
故选D.
根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状 | 浓硫酸具有吸水性和强氧化性 |
| B | 将0.1mol/LMgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶解度比Mg(OH)2的小 |
| C | FeCl3和BaCl2混合溶液中通入足量SO2 | 溶液变为浅绿色且有白色沉淀生成 | Fe3+被还原为Fe2+,沉淀为BaSO3 |
| D | 常温下,将铁片浸入足量浓硫酸中 | 铁片上无明显现象 | 常温下,铁与浓硫酸没有发生化学反应 |
A.A B.B C.C D.D
【考点】U5:化学实验方案的评价.
【分析】A.浓硫酸具有脱水性,可将有机物中的氢氧原子以2:1脱去,表现为强氧化性,在反应中S元素化合价降低,被还原生成二氧化硫;
B.实现了沉淀的转化,说明氢氧化铜更难溶,难溶物的溶度积越小越难溶;
C.二氧化硫被氧化成硫酸,生成的沉淀为硫酸钡;
D.常温下铁与浓硫酸发生了钝化现象,不是不反应.
【解答】解:A.向蔗糖中加入浓硫酸,蔗糖变黑,说明蔗糖被碳化,膨胀并有刺激性气味的气体放出,说明发生氧化还原反应生成二氧化碳、二氧化硫,浓硫酸表现了脱水性和强氧化性,故A错误;
B.将0.1mol•L﹣1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,说明NaOH完全反应,再滴加0.1mol•L﹣1CuSO4溶液,先有白色沉淀生成后变为浅蓝色沉淀,说明发生了沉淀的转化,溶度积大的物质向溶度积小的物质转化,所以Cu(OH)2的溶度积比Mg(OH)2的小,故B正确;
C.FeCl3和BaCl2混合溶液中通入足量SO2,铁离子与二氧化硫发生氧化还原反应,Fe3+被还原为Fe2+,同时生成BaSO4,故C错误;
D.常温下,将铁片浸入足量浓硫酸中,由于发生了钝化现象,阻止了反应的继续进行,并不是不反应,故D错误;
故选B.
本卷还有6题,登录并加入会员即可免费使用哦~

该作品由: 用户黄雯雯分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。






