中国丝绸有五千年的历史和文化.古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层的丝胶蛋白杂质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮.这种“碱剂”可能是( )
A.食盐B.火碱C.草木灰D.胆矾
【考点】酸、碱、盐、氧化物的概念及其相互联系.
【分析】由题意可知,该物质是一种盐,水溶液呈碱性,为强碱弱酸盐来解答.
【解答】解:由题意可知,该物质是一种盐,水溶液呈碱性,为强碱弱酸盐
A.食盐中氯化钠为强酸强碱盐,故A错误;
B.火碱是氢氧化钠,属于碱,故B错误;
C.草木灰中碳酸钾强碱弱酸盐,故C正确;
D.胆矾是硫酸铜晶体,是强酸弱碱盐,故D错误;
故选C.
关于下列图示的说法中,正确的是( )
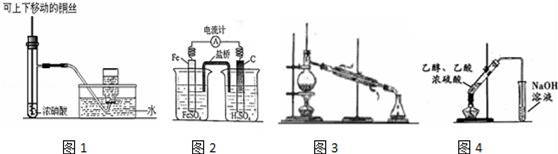

A.图1制备并收集少量NO2气体
B.图2是原电池装置,Fe电极为负极
C.图3常用于分离互不相溶的液体
D.图4可用于实验室制取和收集乙酸乙酯
【考点】化学实验方案的评价;物质的分离、提纯的基本方法选择与应用;常见气体制备原理及装置选择;乙酸乙酯的制取.
【分析】A.NO2易溶于水且和水反应,不能用排水法收集;
B.符合原电池装置,铁为负极被氧化;
C.为蒸馏装置,分离沸点不同的液体混合物;
D.乙酸乙酯在氢氧化钠溶液中可水解.
【解答】解:A.NO2易溶于水且和水反应,不能用排水法收集,应用排空法收集,故A错误;
B.符合原电池装置,铁为负极被氧化,石墨为正极,发生还原反应生成氢气,故B正确;
C.为蒸馏装置,分离沸点不同的液体混合物,互不相溶的液体应用分液的方法分离,故C错误;
D.乙酸乙酯在氢氧化钠溶液中可水解,应用饱和碳酸钠溶液,故D错误.
故选B.
利用如图所示装置进行下列实验,能得出相应实验结论的是( ) 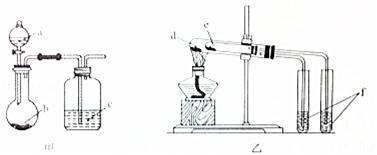

选项
实验试剂
实验结论
A
a.稀硫酸
b.碳酸氢钠
c.硅酸钠溶液
酸性:硫酸>碳酸>硅酸
B
a.稀盐酸
b.二氧化锰
c.溴化钠溶液
氧化性:MnO2>Cl2>Br2
C
d.小苏打
e.苏打
f.石灰水
热稳定性:苏打>小苏打
D
d.氯化钠
e.氯化铵
f.硝酸银溶液
沸点:氯化钠>氯化铵
A.AB.BC.CD.D
【考点】化学实验方案的评价.
【分析】A.强酸能弱酸盐反应生成弱酸,根据强酸制取弱酸判断酸性强弱;
B.稀盐酸和二氧化锰不反应,浓盐酸和二氧化锰在加热条件下反应生成氯气;
C.碳酸钠热稳定性较强,碳酸氢钠不稳定,受热易分解;
D.氯化铵不稳定受热易分解.
【解答】解:A..强酸能弱酸盐反应生成弱酸,根据强酸制取弱酸判断酸性强弱,稀硫酸和碳酸氢钠反应生成二氧化碳,二氧化碳、水和硅酸钠反应生成难溶性硅酸,看到的现象是烧瓶中有气体生成、c中有沉淀生成,所以可以实现实验目的,故A正确;
B.稀盐酸和二氧化锰不反应,浓盐酸和二氧化锰在加热条件下反应生成氯气,所以不能得到氯气,不能实现实验目的,故B错误;
C.碳酸钠热稳定性较强,碳酸氢钠不稳定,受热易分解,所以d为碳酸钠、e为碳酸氢钠,故C错误;
D.氯化铵不稳定受热易分解,所以该装置不能实现实验目的,故D错误;
故选A.
实验室有下列试剂,其中必须用带橡胶塞的试剂瓶保存的是( )
①NaOH溶液 ②水玻璃 ③Na2S溶液 ④Na2CO3溶液 ⑤NH4Cl溶液 ⑥澄清石灰水 ⑦浓HNO3⑧浓H2SO4.
A.①⑥B.①②③④⑥C.①②③⑥⑦⑧D.⑤⑦⑧
【考点】化学试剂的存放.
【分析】玻璃中含有二氧化硅,只要能和二氧化硅反应的药品不能盛放在带有玻璃塞的试剂瓶中,据此分析解答.
【解答】解:①NaOH与二氧化硅反应生成粘性的硅酸钠,导致玻璃塞和试剂瓶粘结在一起而打不开,所以氢氧化钠溶液需放在带橡胶塞的玻璃试剂瓶中;
②Na2SiO3溶液由于弱酸阴离子水解导致溶液显示碱性,可以和玻璃的成分二氧化硅之间反应,所以盛放Na2SiO3等溶液的试剂瓶应用橡皮塞;
③Na2S水解显碱性,与二氧化硅反应,所以Na2S需放在带橡胶塞的玻璃试剂瓶中;
④Na2CO3水解显碱性,与二氧化硅反应硅酸钠和水,所以Na2CO3需放在带橡胶塞的玻璃试剂瓶中;
⑤NH4Cl溶液弱碱阳离子水解导致溶液显示酸性,酸性溶液与玻璃成分不反应,可以存放在玻璃塞的试剂瓶中;
⑥石灰水与二氧化硅反应硅酸钙和水,所以石灰水需放在带橡胶塞的玻璃试剂瓶中;
⑦浓HNO3溶液显示酸性,酸性溶液与玻璃成分不反应,可以存放在玻璃塞的试剂瓶中;
⑧浓H2SO4溶液显示酸性,酸性溶液与玻璃成分不反应,可以存放在玻璃塞的试剂瓶中.
故选B.
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是( )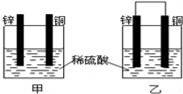

A.装置甲中铜片表面产生气泡
B.装置甲溶液中SO42ˉ向铜片做定向移动
C.装置乙中电子从铜片经导线流向锌片
D.装置乙中正极的电极反应式:2H++2eˉ═H2↑
【考点】原电池和电解池的工作原理.
【分析】锌比铜活泼,能与稀硫酸反应,铜为金属活动性顺序表H元素之后的金属,不能与稀硫酸反应,甲没有形成闭合回路,不能形成原电池,乙形成闭合回路,形成原电池,根据原电池的组成条件和工作原理解答该题.
【解答】解:A.甲没有形成原电池,铜为金属活动性顺序表H元素之后的金属,不能与稀硫酸反应,甲烧杯中铜片表面没有气泡产生,故A错误;
B.原电池工作时阴离子向负极移动,故B错误;
C.锌为负极,电子从锌经导线流向铜,故C错误;
D.透过为正极,正极上氢离子得到电子被还原生成氢气,故D正确.
故选D.
本卷还有23题,登录并加入会员即可免费使用哦~

该作品由: 用户张三分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。