298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
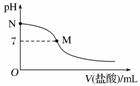
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH![]() )=c(Cl-)=c(H+)=c(OH-)
)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
D [A项,盐酸滴定氨水时,滴定终点溶液为NH4Cl溶液,呈酸性,故指示剂应选甲基橙,错误;B项,一水合氨属于弱碱,与盐酸正好反应生成NH4Cl时溶液呈酸性,故二者等浓度反应时,若溶液的pH=7,盐酸的体积应小于氨水的体积,即小于20.0 mL,错误;C项,根据电荷守恒可知溶液中:c(NH![]() )+c(H+)=c(Cl-)+c(OH-),M点溶液的pH=7,即c(H+)=c(OH-),则c(NH
)+c(H+)=c(Cl-)+c(OH-),M点溶液的pH=7,即c(H+)=c(OH-),则c(NH![]() )=c(Cl-),由于水的电离是微弱的,故c(NH
)=c(Cl-),由于水的电离是微弱的,故c(NH![]() )=c(Cl-)>c(H+)=c(OH-),错误;D项,由图可知,N点即为0.10 mol·L-1氨水,由其电离度为1.32%,可知0.10 mol·L-1氨水中c(OH-)=0.001 32 mol·L-1,故该氨水中11<pH<12,正确。]
)=c(Cl-)>c(H+)=c(OH-),错误;D项,由图可知,N点即为0.10 mol·L-1氨水,由其电离度为1.32%,可知0.10 mol·L-1氨水中c(OH-)=0.001 32 mol·L-1,故该氨水中11<pH<12,正确。]
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
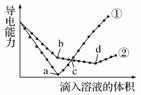
下列分析不正确的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.c点,两溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性
C [试题所涉及的化学方程式为:向Ba(OH)2溶液中滴入H2SO4溶液,Ba(OH)2+H2SO4===BaSO4↓+2H2O(反应ⅰ);向Ba(OH)2溶液中滴入NaHSO4溶液,Ba(OH)2+NaHSO4===BaSO4↓+NaOH+H2O(反应ⅱ),NaOH+NaHSO4===Na2SO4+H2O(反应ⅲ)。 A项,由题图可知曲线①在a点溶液导电能力最低,说明此时溶液中离子浓度最小,当Ba(OH)2和H2SO4完全反应时生成BaSO4沉淀,此时溶液导电能力最低,故反应ⅰ符合,正确;B项,曲线②中b点进行的反应是反应ⅱ,溶液中含有Ba(OH)2与NaHSO4反应生成的NaOH,正确;C项,c点曲线①表示Ba(OH)2已经完全反应,并剩余H2SO4,溶液显酸性,c点曲线②表示NaOH与NaHSO4反应,且NaOH还有剩余,故溶液中含有反应ⅲ生成的Na2SO4和剩余的NaOH,溶液显碱性,所以c点两溶液中含有OH-的量不相同,错误;D项,a点为Ba(OH)2和 H2SO4完全反应时生成BaSO4沉淀,溶液呈中性,d点溶液中溶质只有Na2SO4,溶液也呈中性,正确。]
下列曲线中,可以描述乙酸(甲,Ka=1.8×10-5)和一氯乙酸(乙,Kb=1.4×10-3)在水中的电离度与浓度关系的是( )
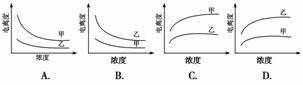
B [根据甲、乙的电离平衡常数得,这两种物质都是弱电解质,在温度不变、浓度相等时,电离程度CH3COOH<CH2ClCOOH,可以排除A、C;当浓度增大时,物质的电离程度减小,排除D选项,故B项正确。]
浓度均为0.10 mol·L-1、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
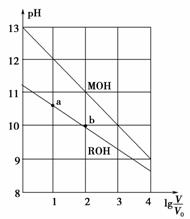
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg![]() =2时,若两溶液同时升高温度,则c(M+)/c(R+)增大
=2时,若两溶液同时升高温度,则c(M+)/c(R+)增大
D [A项,0.10 mol·L-1的MOH和ROH,前者pH=13,后者pH小于13,说明前者是强碱,后者是弱碱,正确;B项,ROH是弱碱,加水稀释,促进电离,b点电离程度大于a点,正确;C项,两碱溶液无限稀释,溶液近似呈中性,c(OH-)相等,正确;D项,由MOH是强碱,在溶液中完全电离,所以c(M+)不变,ROH是弱碱,升高温度,促进电离平衡ROH![]() R++OH-向右进行,c(R+)增大,所以
R++OH-向右进行,c(R+)增大,所以![]() 减小,错误。]
减小,错误。]
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
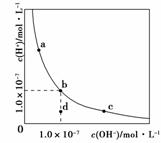
C [A项,升高温度,促进水的电离平衡,则c(H+)和c(OH-)都同等程度地变大,若由c向b变化,则c(H+)增大,c(OH-)将变小,错误;B项,根据b点对应的c(H+)和c(OH-)都为1.0×10-7 mol/L,所以该温度下,水的离子积常数Kw=1.0×10-7×1.0×10-7=1.0×10-14,错误;C项,加入FeCl3发生水解反应:Fe3++3H2O![]() Fe(OH)3+3H+,破坏水的电离平衡,c(H+)增大、Kw不变,c(OH-)变小,则可能引起由b向a变化,正确;D项,c点对应的溶液呈碱性,稀释溶液,c(OH-)变小,Kw不变,c(H+)增大,故可引起由c向b的变化,而不是向d变化,错误。]
Fe(OH)3+3H+,破坏水的电离平衡,c(H+)增大、Kw不变,c(OH-)变小,则可能引起由b向a变化,正确;D项,c点对应的溶液呈碱性,稀释溶液,c(OH-)变小,Kw不变,c(H+)增大,故可引起由c向b的变化,而不是向d变化,错误。]
本卷还有25题,登录并加入会员即可免费使用哦~

该作品由: 用户杨泉分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。