生活中的问题常涉及到化学知识,下列叙述中正确的是( )
A.硫酸钡是一种难溶于水和酸的盐,可用作X光透视肠胃的药剂
B.使用明矾可以对水进行消毒、杀菌
C.铁制品在干燥的空气中易生锈
D.棉花、蚕丝和人造丝的主要成分是纤维素
【考点】药物的主要成分和疗效;金属的电化学腐蚀与防护;盐类水解的应用;纤维素的性质和用途.
【专题】元素及其化合物;有机化学基础.
【分析】A.难溶于水也难溶于酸的BaSO4,不但没有毒,而且它具有不易被X射线透过的特点;
B.明矾中的铝离子水解生成氢氧化铝胶体只具有吸附杂质的作用;
C.铁在有水和氧气并存时易生锈;
D.蚕丝的成分是蛋白质.
【解答】解:A.溶于水的钡盐[如Ba(NO3)2、BaCl2等]对人体有毒,但是难溶于水也难溶于酸的BaSO4,不但没有毒,而且还由于它具有不易被X射线透过的特点,在医疗上被用作X射线透视胃肠的内服药剂﹣﹣“钡餐”,故A正确;
B.明矾利用铝离子水解生成氢氧化铝胶体能吸附悬浮的杂质可以净水,但不能杀菌消毒,故B错误;
C.在干燥的空气中,铁不与水接触,不易生锈,故C错误;
D.棉花和人造丝的主要成分都是纤维素,蚕丝的成分是蛋白质,故D错误.
故选A.
【点评】本题考查钡餐、明矾净水、原电池和物质的成分,难度不大,明确铁生锈原理是解题的关键.
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀
C.电解MgCl2饱和溶液,可制得金属镁
D.MgO的熔点很高,可用于制作耐高温材料
【考点】金属的电化学腐蚀与防护;金属冶炼的一般原理;镁、铝的重要化合物.
【专题】电化学专题;几种重要的金属及其化合物.
【分析】A、胶体能净化水;
B、锌块作原电池负极被腐蚀,从而保护铁被腐蚀;
C、活泼金属采用电解其熔融盐的方法冶炼;
D、根据氧化镁的性质判断其用途.
【解答】解:A、明矾中含有铝元素,铝能水解生成氢氧化铝胶体,胶体具有吸附性而吸附水中的悬浮物所以能净水,故A正确;
B、锌、铁和海水构成原电池,锌作负极,铁作正极,负极锌失电子被腐蚀,从而保护了铁被腐蚀,故B正确;
C、镁是活泼金属,电解其水溶液时,阴极上氢离子得电子而不是镁离子得电子,所以得不到金属镁,应采用电解其熔融盐的方法冶炼,故C错误;
D、氧化镁的熔点较高,所以能制作耐高温材料,故D正确.
故选:C.
【点评】本题考查了化学知识在日常生活中的应用,难度不大,易错选项是A,注意氢氧化铝胶体具有吸附性.
Na、Al、Fe、Cu都是重要的金属,下列有关它们的说法正确的是( )
A.在一定条件下都能与水发生置换反应
B.在一定条件下都能与稀HNO3发生氧化还原反应
C.都必须隔绝空气保存
D.在一定条件下都能与稀H2SO4反应产生H2
【考点】常见金属元素的单质及其化合物的综合应用.
【专题】几种重要的金属及其化合物.
【分析】A、Cu不能与水发生置换反应;
B、Na、Al、Fe、Cu都有强还原性能与氧化性的稀HNO3发生氧化还原反应;
C、铝表面形成致密的氧化膜,不需隔绝空气保存;
D、铜不与稀硝酸反应.
【解答】解: A、Cu不能与水发生置换反应,故A不选;
B、Na、Al、Fe、Cu都有强还原性能与氧化性的稀HNO3发生氧化还原反应,故B符合;
C、铝表面形成致密的氧化膜,不需隔绝空气保存,故C不选;
D、铜不与稀硝酸反应,故D不选;
故选B.
【点评】本题考查常见的金属单质的性质,为高频考点,把握金属及其化合物性质为解答的关键,综合性较强,题目难度不大.
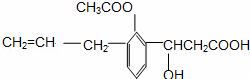
某有机物的结构简式如图,则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解⑥氧化 ⑦中和( )
A.①②③⑤⑥ B.②③④⑤⑥ C.①②③④⑤⑥ D.①②③④⑤⑥⑦
【考点】有机物的结构和性质.
【分析】由结构简式可知,该有机物中含有碳碳双键、酯基、﹣OH、﹣COOH,结合烯烃、酯、醇、羧酸的性质来解答.
【解答】解:①因含有羟基、羧基,则能发生取代反应,故①选;
②因含有碳碳双键和苯环,能发生加成反应,故②选;
③因与﹣OH相连的C的邻位碳原子上有H原子,则能发生消去反应,故③选;
④因含有羟基、羧基,则能发生酯化反应,故④选;
⑤含有酯基,则能发生水解反应,故⑤选;
⑥含有碳碳双键、﹣OH,能发生氧化反应,故⑥选;
⑦因含有羧基,则能发生中和反应,⑦选;
故选D.
【点评】本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酯、醇、羧酸的性质及反应的考查,题目难度不大.
在下列条件下,能大量共存的微粒组是( )
| 化学式 | 电离常数 |
| CH3COOH | Ki=1.7×10﹣5 |
| HClO | Ki=3.0×10﹣8 |
| H2CO3 | Ki1=4.3×10﹣7 Ki2=5.6×10﹣11 |
A.c(H+)=1×10﹣14mol/L的溶液:K+、Na+、AlO2﹣、S2O32﹣
B.右表提供的数据下:HClO、HCO3﹣、ClO﹣、CO32﹣
C.能与Al反应生成H2的溶液:NH4+、Ca2+、NO3﹣、I﹣
D.中性的溶液中:CO32﹣、Na+、SO42﹣、AlO2﹣
【考点】离子共存问题.
【专题】离子反应专题.
【分析】A.c(H+)=1×10﹣14mol/L的溶液,显碱性;
B.由表中的数据可知,酸性HClO>CO32﹣;
C.与Al反应生成H2的溶液,为非氧化性酸或强碱溶液;
D.中性溶液中不能存在水解显碱性的离子.
【解答】解:A.c(H+)=1×10﹣14mol/L的溶液,显碱性,该组离子之间不反应,可大量共存,故A正确;
B.由表中的数据可知,酸性HClO>CO32﹣,二者发生强酸制取弱酸的反应,不能共存,故B错误;
C.与Al反应生成H2的溶液,为非氧化性酸或强碱溶液,碱溶液中不能存在NH4+,酸溶液中NO3﹣、I﹣(或Al)发生氧化还原反应,不能共存,故C错误;
D.CO32﹣、AlO2﹣均水解显碱性,与中性溶液不符,故D错误;
故选A.
【点评】本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,选项BD为解答的关键,注意选项B中表格数据的应用,题目难度不大.
本卷还有16题,登录并加入会员即可免费使用哦~

该作品由: 用户lk分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。