生活中处处有化学,下列叙述正确的是
A . HB 铅笔芯的成分为二氧化铅 B .碳酸氢钠可做食品膨松剂
C .青铜和黄铜是不同结构的单质铜 D .焰火中红色来源于钠盐灼烧
B
【详解】 A .铅笔芯的主要成分为石墨,不含二氧化铅, A 错误;
B .碳酸氢钠不稳定,受热易分解产生二氧化碳,能使面团松软,可做食品膨松剂, B 正确 ;
C .青铜是在纯铜 ( 紫铜 ) 中加入锡或铅的合金,黄铜为是由铜和锌所组成的合金,两者均属于混合物,不是铜单质, C 错误;
D .钠元素灼烧显黄色, D 错误;
故选 B 。
一种实现二氧化碳固定及再利用的反应如下:
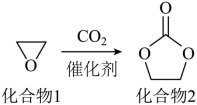
下列叙述正确的是
A .化合物 1 分子中的所有原子共平面 B .化合物 1 与乙醇互为同系物
C .化合物 2 分子中含有羟基和酯基 D .化合物 2 可以发生开环聚合反应
D
【详解】 A .化合物 1 分子中还有亚甲基结构,其中心碳原子采用 sp 3 杂化方式,所以所有原子不可能共平面, A 错误;
B .结构相似,分子上相差 n 个 CH 2 的有机物互为同系物,上述化合物 1 为环氧乙烷,属于醚类,乙醇属于醇类,与乙醇结构不相似,不是同系物, B 错误;
C .根据上述化合物 2 的分子结构可知,分子中含酯基,不含羟基, C 错误;
D .化合物 2 分子可发生开环聚合形成高分子化合物  , D 正确;
, D 正确;
答案选 D 。
某白色粉末样品,可能含有 、
、
和
。取少量样品进行如下实验:
① 溶于水,得到无色透明溶液
② 向 ① 的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③ 取 ② 的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A . B .
C .
D .
A
【详解】由题意可知, ① 取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存, ② 向 ① 的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在 Na 2 S 2 O 3 , 发生反应 S 2 O +2H + =S↓+H 2 O+SO 2 ↑ ,离心分离, ③ 取 ② 的上层清液,向其中滴加 BaCl 2 溶液,有沉淀生成,则沉淀为 BaSO 4 ,说明固体中存在 Na 2 SO 4 ,不能确定是否有 Na 2 SO 3 和 Na 2 CO 3 , Na 2 SO 3 与过量盐酸反应生成二氧化硫, Na 2 CO 3 与过量盐酸反应生成二氧化碳,而这些现象可以被 Na 2 S 2 O 3 与过量盐酸反应的现象覆盖掉,综上分析,该样品中确定存在的是: Na 2 SO 4 、 Na 2 S 2 O 3 ,
答案选 A 。
由实验操作和现象,可得出相应正确结论的是
| | 实验操作 | 现象 | 结论 |
| A | 向 NaBr 溶液中滴加过量氯水,再加入淀粉 KI 溶液 | 先变橙色,后变蓝色 | 氧化性: |
| B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入少量新制的 | 无砖红色沉淀 | 蔗糖未发生水解 |
| C | 石蜡油加强热,将产生的气体通入 | 溶液红棕色变无色 | 气体中含有不饱和烃 |
| D | 加热试管中的聚氯乙烯薄膜碎片 | 试管口润湿的蓝色石蕊试纸变红 | 氯乙烯加聚是可逆反应 |
A . A B . B C . C D . D
C
【详解】 A .向 NaBr 溶液中滴加过量氯水,溴离子被氧化为溴单质,但氯水过量,再加入淀粉 KI 溶液,过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质, A 错误;
B .向蔗糖溶液中滴加稀硫酸,水浴加热后,应加入氢氧化钠溶液使体系呈碱性,若不加氢氧化钠,未反应的稀硫酸会和新制氢氧化铜反应,则不会产生砖红色沉淀,不能说明蔗糖没有发生水解, B 错误;
C .石蜡油加强热,产生的气体能使溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,与溴发生加成反应使溴的四氯化碳溶液褪色, C 正确;
D .聚氯乙烯加强热产生能使湿润蓝色石蕊试纸变红的气体,说明产生了氯化氢,不能说明氯乙烯加聚是可逆反应,可逆反应是指在同一条件下,既能向正反应方向进行,同时又能向逆反应的方向进行的反应,而氯乙烯加聚和聚氯乙烯加强热分解条件不同, D 错误;
答案选 C 。
化合物 可用于电讯器材、高级玻璃的制造。 W 、 X 、 Y 、 Z 为短周期元素,原子序数依次增加,且加和为 21 。
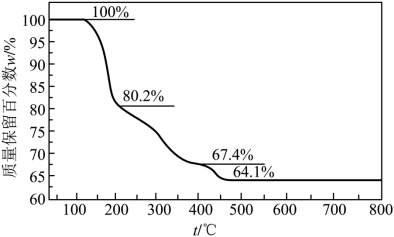
分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在
以下热分解时无刺激性气体逸出。下列叙述正确的是
A . W 、 X 、 Y 、 Z 的单质常温下均为气体
B .最高价氧化物的水化物的酸性:
C . 阶段热分解失去 4 个
D . 热分解后生成固体化合物
D
【分析】化合物 (YW 4 X 5 Z 8 ·4W 2 Z) 可用于电讯器材、高级玻璃的制造。 W 、 X 、 Y 、 Z 为短周期元素,原子序数依次增加,且加和为 21 。该化合物的热重曲线如图所示,在 200℃ 以下热分解时无刺激性气体逸出,则说明失去的是水,即 W 为 H , Z 为 O , YZ 2 分子的总电子数为奇数,常温下为气体,则 Y 为 N ,原子序数依次增加,且加和为 21 ,则 X 为 B 。
【详解】 A . X(B) 的单质常温下为固体,故 A 错误;
B .根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性: X(H 3 BO 3 ) < Y(HNO 3 ) ,故 B 错误;
C .根据前面已知 200℃ 以下热分解时无刺激性气体逸出,则说明失去的是水,若 100 ~ 200℃ 阶段热分解失去 4 个 H 2 O ,则质量分数 ,则说明不是失去 4 个 H 2 O ,故 C 错误;
D .化合物 (NH 4 B 5 O 8 ·4H 2 O) 在 500℃ 热分解后若生成固体化合物 X 2 Z 3 (B 2 O 3 ) ,根据硼元素守恒,则得到关系式 2NH 4 B 5 O 8 ·4H 2 O ~ 5B 2 O 3 ,则固体化合物 B 2 O 3 质量分数为 ,说明假设正确,故 D 正确。
综上所述,答案为 D 。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户莫分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。