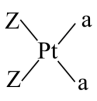
顺铂为一种配合物,其结构如图所示,其中心离子为 。已知 X 、 Y 、 Z 是原子半径依次增大的不同短周期元素, X 、 Z 的原子核外都有一个未成对电子, Y 的第一电离能比同周期左右相邻元素的大, a 分子是由 X 、 Y 元素组成的四原子分子。下列有关叙述正确的是
A .顺铂的空间结构中 位于正四面体的中心
B . a 分子的 VSEPR 模型是正四面体形,其键角为
C . Y 的氧化物对应的水化物是强酸
D .由 X 、 Y 、 Z 三种元素组成的化合物中可能含有离子键,也可能不含离子键
D
【分析】由题意知,顺铂中 Z 显- 1 价, Z 可能为 F 或 Cl , Y 的第一电离能比同周期左右相邻元素的大,且 Y 与 X 能形成四原子分子, Y 可能为 N 或 P ,则 X 为 H ;又因为 X 、 Y 、 Z 的原子半径依次增大,可推知 X 为 H , Y 为 N , Z 为 Cl , a 为 NH 3 。
【详解】 A .顺铂中 与 2 个 Cl ¯ 、 2 个 NH 3 形成配位键,其空间结构不是正四面体形, A 错误;
B . NH 3 中 N 的价层电子对数 = , N 原子上有一对孤电子对,所以 NH 3 的 VSEPR 模型是四面体形,由于孤电子对与成键电子对之间斥力更大,分子中键角小于
, B 错误;
C . Y(N) 的氧化物对应的水化物可以是 HNO 3 ( 强酸 ) 或 HNO 2 ( 弱酸 ) , C 错误;
D . X 、 Y 、 Z 三种元素组成的化合物可以是 NH 4 Cl( 含离子键 ) ,也可以是 NH 2 Cl( 不含离子键 ) , D 正确;故选 D 。
【点睛】第一电离能比同周期左右相邻元素的大,一般是第 ⅡA 族或第 ⅤA 族元素。
下列 “ 类比 ” 结果正确的是
A .苯不能使酸性 KMnO 4 溶液褪色,甲苯也不能使酸性 KMnO 4 溶液褪色
B . NH 3 的分子构型为三角锥形, PCl 3 的分子构型也为三角锥形
C . Ca(HCO 3 ) 2 的溶解度比 CaCO 3 的大, NaHCO 3 的溶解度也比 Na 2 CO 3 的大
D . Na 2 O 2 与 CO 2 反应生成 Na 2 CO 3 与 O 2 , Na 2 O 2 与 SO 2 反应生成 Na 2 SO 3 与 O 2
B
【详解】 A .苯不与酸性高锰酸钾溶液反应,甲苯可与酸性高锰酸钾溶液反应从而使其褪色, A 错误;
B . NH 3 中 N 原子的价层电子对数为 3+ =4 , PCl 3 中 P 原子的价层电子对数也是 3+
=4 ,两者均有一对孤电子对,分子构型为三角锥形, B 正确;
C .碳酸氢钠的溶解度小于 Na 2 CO 3 , C 错误;
D . Na 2 O 2 具有强氧化性, SO 2 具有较强的还原性,两者反应生成 Na 2 SO 4 , D 错误;
故答案选 B 。
下列有关说法不正确的是
A . NaBr 属于离子化合物 B . HCl 分子中含极性共价键
C .热稳定性: D .卤族元素在自然界中都以化合态存在
C
【详解】 A . NaBr 属于离子化合物, A 正确;
B . HCl 分子中 H 和 Cl 电负性不同,其分子中含极性共价键, B 正确;
C .元素的非金属性越强,则其简单氢化物的热稳定性越强,则热稳定性 HI<HBr<HCl<HF , C 错误;
D .卤素原子最外层有 7 个电子,极易得到电子形成 8 电子稳定结构,所以卤族元素只以化合态存在于自然界中, D 正确;
故答案选 C 。
下列现象与氢键有关的是
①H 2 O 的熔、沸点比 VIA 族其它元素氢化物的高
② 水分子高温下也很稳定
③ 接近水的沸点的水蒸气的相对分子质量测定值比用化学式 H 2 O 计算出来的相对分子质量大一些
④ 邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A . ①②③④ B . ①③④ C . ①②③ D . ①②④
B
【详解】 ① 水分子之间能形成氢键,所以常温常压下, H 2 O 的熔、沸点比第 VIA 族其它元素氢化物的高, ① 正确;
② 水分子高温下也很稳定与氧元素的非金属性强,氢氧键的键能大有关,与氢键无关, ② 错误;
③ 接近水的沸点的水蒸气的相对分子质量测定值比用化学式 H 2 O 计算出来的相对分子质量大一些,其主要原因是接近水的沸点的水蒸气中水分子间因氢键而形成了 “ 缔合分子 ” , ③ 正确;
④ 邻羟基苯甲酸能形成分子内氢键,对羟基苯甲酸能形成分子间氢键,则邻羟基苯甲酸的分子间作用力小于对羟基苯甲酸,熔、沸点低于羟基苯甲酸,所以邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低与氢键有关, ④ 正确;
正确的是: ①③④ ;
故选 B 。
光气 ( ) 是一种重要的有机中间体。反应
可用于制备光气。下列有关叙述错误的是
A .氧原子的结构示意图为  B .
B . 的电子式为
![]()
C . 为极性分子 D .
中碳原子的轨道杂化类型为
杂化
A
【详解】 A .氧原子的结构示意图为 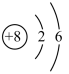 , A 错误;
, A 错误;
B . 分子中存在过氧键,电子式为
, B 正确;
C . 不是正四面体,正负电荷中心不重合, C 正确;
D . 中有一个
键和两个 C—Cl 键,碳原子的轨道杂化类型为
杂化, D 正确;
故选 A 。
本卷还有30题,登录并加入会员即可免费使用哦~

该作品由: 用户laiqingdong 分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。