化学科学与社会活动密切相关。下述措施应积极推广的是
A . 在抗击新冠肺炎疫情斗争中,提高环境友好无残留消毒剂的使用比例
B . 原料药生产厂通过蒸发与焚烧过程,处理其生产废液
C . 海边建筑工程施工,就近取海水海沙生产混凝土
D . 为保证食物的口感与风味,增加食品添加剂使用品种与数量
A
【详解】
A. 使用环境友好无残留消毒剂,可以减少或杜绝污染,应该积极推广,故 A 正确;
B. 原料药生产厂生产的废液要集体利用物理、化学和生物的方法处理,不能蒸发和焚烧,故 B 错误;
C. 海边建筑工程施工,就近取海水海沙生产混凝土,会造成海洋生态环境的污染和破坏,故 C 错误;
D. 食品添加剂使用品种与数量都有严格的使用标准,不能随意增加,故 D 错误;
故选 A 。
利用下列装置 ( 夹持装置略 ) 进行实验,能达到实验目的的是
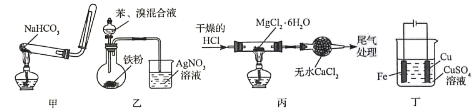
A . 用甲装置制备并收集 CO 2
B . 用乙装置制备溴苯并验证有 HBr 产生
C . 用丙装置制备无水 MgCl 2
D . 用丁装置在铁上镀铜
C
【详解】
A. CO 2 密度大于空气,应采用向上排空气法收集, A 错误;
B. 苯与溴在溴化铁作用下反应,反应较剧烈,反应放热,且溴易挥发,挥发出来的溴单质能与水反应生成氢溴酸,所以验证反应生成的 HBr ,应先将气体通过四氯化碳,将挥发的溴单质除去, B 错误;
C. MgCl 2 能水解,在加热时通入干燥的 HCl ,能避免 MgCl 2 的水解, C 正确;
D. 电解时,阳极发生氧化反应,阴极发生还原反应,所以丁装置铁为阳极,失去电子,生成二价铁离子,铜为阴极,溶液中的铜离子得到电子,得到铜, D 错误。
答案选 C 。
【点睛】
本题为实验题,结合物质的性质和电解的原理进行解题,掌握常见物质的制备方法,注意水解的知识点。
能正确表示下列反应的离子方程式是
A . 溶液与少量
溶液反应:
B . 电解 水溶液:
C . 乙酸乙酯与 溶液共热:
D . 溶液中滴加稀氨水:
C
【详解】
A . (NH 4 ) 2 Fe(SO 4 ) 2 可以写成 (NH 4 ) 2 SO 4 ‧ FeSO 4 , (NH 4 ) 2 Fe(SO 4 ) 2 溶液与少量 Ba(OH) 2 溶液反应, OH - 先与 Fe 2+ 反应,再和 反应,由于 Ba(OH) 2 较少,
不会参与反应,离子方程式为: Fe 2+ +
+ Ba 2+ + 2OH - =Fe(OH) 2 ↓+BaSO 4 ↓ , A 错误;
B .用惰性材料为电极电解 MgCl 2 溶液,阳极反应为: 2Cl - -2e - =Cl 2 ↑ ,阴极反应为: 2H 2 O+2e - +Mg 2+ =Mg(OH) 2 ↓+H 2 ↑ ,总反应的离子方程式为: Mg 2+ +2Cl - +2H 2 O= Mg(OH) 2 ↓+H 2 ↑+ Cl 2 ↑ , B 错误;
C .乙酸乙酯与氢氧化钠溶液共热时发生水解,生成乙酸钠和乙醇,离子方程式为: CH 3 COOCH 2 CH 3 +OH - ![]() CH 3 COO - +CH 3 CH 2 OH , C 正确;
CH 3 COO - +CH 3 CH 2 OH , C 正确;
D .向硫酸铜溶液中滴加氨水,氨水与硫酸铜发生复分解反应生成氢氧化铜沉淀和硫酸铵,一水合氨为弱电解质,在离子反应中不能拆开,离子方程式为: Cu 2+ +2NH 3 •H 2 O=2 +Cu(OH) 2 ↓ , D 错误。
答案选 C 。
紫花前胡醇 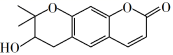 可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述错误的是
可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述错误的是
A . 分子式为 C 14 H 14 O 4
B . 不能使酸性重铬酸钾溶液变色
C . 能够发生水解反应
D . 能够发生消去反应生成双键
B
【详解】
A. 根据该有机物的分子结构可以确定其分子式为 C 14 H 14 O 4 , A 叙述正确;
B. 该有机物的分子在有羟基,且与羟基相连的碳原子上有氢原子,故其可以被酸性重铬酸钾溶液氧化,能使酸性重铬酸钾溶液变色, B 叙述不正确;
C. 该有机物的分子中有酯基,故其能够发生水解反应, C 叙述正确;
D. 该有机物分子中与羟基相连的碳原子的邻位碳原子上有氢原子,故其可以在一定的条件下发生消去反应生成碳碳双键, D 叙述正确。
综上所述,故选 B 。
X 、 Y 、 Z 、 M 、 Q 五种短周期元素,原子序数依次增大。 Y 元素的最高正价为 价, Y 元素与 Z 、 M 元素相邻,且与 M 元素同主族;化合物
的电子总数为 18 个; Q 元素的原子最外层电子数比次外层少一个电子。下列说法 不正确 的是
A . 原子半径:
B . 最高价氧化物对应水化物的酸性:
C . 易溶于水,其水溶液呈碱性
D . X 、 Z 和 Q 三种元素形成的化合物一定是共价化合物
D
【分析】
X 、 Y 、 Z 、 M 、 Q 为五种短周期元素,原子序数依次增大。 Y 元素的最高正价为 +4 价,则证明该元素为第 IVA 族元素,又知 Y 元素与 Z 、 M 元素相邻,且与 M 同族,则在元素周期表位置应为
| IVA 族 | VA 族 |
| Y | Z |
| M | |
,故推知 Y 为 C 元素, Z 为 N 元素, M 为 Si 元素;化合物 Z 2 X 4 的电子总数为 18 ,则推知, X 为 H ,该化合物为 N 2 H 4 ; Q 元素的原子最外层电子总数比次外层电子数少一个电子,推出 Q 为 Cl 元素,据此结合元素周期律与物质的结构与性质分析作答。
【详解】
根据上述分析可知, X 为 H 、 Y 为 C 元素、 Z 为 N 元素、 M 为 Si 元素、 Q 为 Cl 元素,则
A. 同周期元素从左到右原子半径依次减小,同主族元素从上到下原子半径依次增大,则原子半径比较: Z(N)<Y(C)<M(Si) ,故 A 正确;
B. 同周期元素从左到右元素非金属性依次增强,同主族元素从上到下元素非金属性依次减弱,因元素的非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性: Z(N) > Y(C) > M(Si) ,则最高价氧化物对应水化物的酸性: Z(N) > Y(C) > M(Si) ,故 B 正确;
C. N 2 H 4 的结构简式可表示为 H 2 N-NH 2 ,分子中含两个氨基,可与酸反应,具有碱性,且该分子具有极性,与水分子间也存在氢键,根据相似原理可知, N 2 H 4 易溶于水,故 C 正确;
D. X 、 Z 和 Q 三种元素组成的化合物有很多,不一定都是共价化合物,如氯化铵属于铵盐,为离子化合物,故 D 错误;
答案选 D 。
本卷还有30题,登录并加入会员即可免费使用哦~

该作品由: 用户一顽石分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。