 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中正确的是
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中正确的是
A.x是正极,y是负极
B.x是负极,y是正极。
C.a极和Pt都有气泡产生。
D.CuSO4溶液pH值保持不变,U形管溶液pH值增大。
BC
右图中A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为______________极
(2)滤纸B上发生的总化学方程式为: 。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为:_________________________ ,电极f上发生的反应为:_____________________,槽中盛放的电镀液可以是____________溶液。
(1)正
(2)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3)Zn→Zn2++2e- Zn2++2e-→Zn ZnSO4
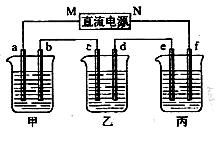 右图所示装置中, 甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
右图所示装置中, 甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:甲溶液 ;乙溶液 ; 丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
(1)①正极 ②4OH--4e-=2H2O + O2↑。
③水减少的质量:![]()
生成O2体积:![]()
④16g
⑤碱性增大,因为电解后,水量减少溶液中NaOH浓度增大
酸性增大,因为阳极上OH-生成O2,溶液中H+离子浓度增大
酸碱性大小没有变化,因为K2SO4是强酸强碱盐,浓度增加不影响溶液的酸碱性
(2)能继续进行,因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应。
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,
原因是 (用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的______。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4 溶液中电解,铝材表面形成氧化膜,阳极电极反应为 。取少量废电解液,加入NaHCO,溶液后产生气泡和白色沉淀,产生沉淀的原因是 。
 (2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 。
(3)利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为
。
(1)①2Al +6H2O + 2OH- = 2[Al(OH)4]- + 3H2 b
② 2Al-6e- +3H2O→ Al2O3 +6H+
与废电解液中的H+反应,使H+浓度减小,产生Al(OH)3沉淀。
(2)补充溶液中的Cu2+
(3)N 牺牲阳极保护法
图中X、Y分别是直流电源的两极,通电后发现 a 极板质量增加, b 极板处有无色无味的气体放出,符合这一情况的是下图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,符合这一情况的是( )。

A
本卷还有9题,登录并加入会员即可免费使用哦~

该作品由: 用户贺培分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。