热化学方程式C(s)+H2O(g)![]() CO(g)+H2(g);△H =+131.3kJ/mol表示( )
CO(g)+H2(g);△H =+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
依据反应热的概念,表示按照方程式系数的物质的量反应时吸收或放出的热量,单位是kJ・mol-1,该方程式表示:1mol碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸收131.3kJ的热量。特别要指明水的状态。
已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625kJ・g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H =-890kJ/mol
B. ![]() CH4(g)+O2(g)=
CH4(g)+O2(g)=![]() CO2(g)+H2O(l);△H =-445kJ/mol
CO2(g)+H2O(l);△H =-445kJ/mol
C.![]()
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-55.625kJ/mol
D
题目中给出的数据意义是:燃烧1g的甲烷放出55.625kJ的热量,应该换算成燃烧1mol甲烷放出的热量为890kJ。热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ・mol-1其他系数与热量相对应的方程式均正确。
在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需117kJ/mol~125KJ/mol的热量,但1,3―环己二烯失去2个氢原子变成苯是放热反应,△H =-23.4kJ/mol,以上事实表明( )
A.1,3―环己二烯加氢是吸热反应
B.苯加氢生成环己烷是吸热反应
C.1,3―环己二烯比苯稳定
D.苯比1,3―环己二烯稳定
D
由题可知:![]() ,因为苯的能量比环己二烯能量低,故苯比环己二烯稳定,故C错;环己二烯加氢是放热过程,A错;苯加氢到环己烷由上图可知是放热过程,B错。
,因为苯的能量比环己二烯能量低,故苯比环己二烯稳定,故C错;环己二烯加氢是放热过程,A错;苯加氢到环己烷由上图可知是放热过程,B错。
在同温同压下,下列各组热化学方程式Q2>Q1的是( )
A.2H2(g)+O2(g)=2H2O(l);△H=-Q1
2H2(g)+O2(g)=2H2O(g);△H=-Q2
B.S(g)+O2(g)=SO2(g);△H=-Q1
S(s)+O2(g)=SO2(g);△H=-Q2
C.![]()
C(s)+O2(g)=CO2(g);△H=-Q2
D.H2(g)+Cl2(g)=2HCl(g);△H=-Q1
![]()
C
反应放出或吸收的热量的多少,跟反应物和生成物的聚集状态有密切关系。A中两式仅生成物中水的状态不同,由于生成液态水比生成气态水放热多,所以Q1>Q2;B中两式仅硫的状态不同,由于固态硫变成气态硫要吸收热量,所以Q1>Q2;C中固态碳与氧气完全反应生成二氧化碳,放出的热量Q2应大于不完全燃烧时生成一氧化碳放出的热量Q1;D中二式各物质的量不同,有Q1=2Q2的关系,故本题的答案应为C。
100gC不完全燃烧所得产物中,CO所占体积为1/3,CO2为2/3,且:
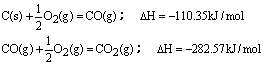
与这些碳完全燃烧相比,损失的热量为( )
A.39.292kJ B.3274.3kJ C.784.92kJ D.2489.44kJ
C
在100gC中有 ![]() 变为CO,有
变为CO,有 ![]() 变为CO2,故与C完全燃烧相比,损失的热量就是CO继续燃烧放出的热量,依据热化学方程式,知损失的热量为
变为CO2,故与C完全燃烧相比,损失的热量就是CO继续燃烧放出的热量,依据热化学方程式,知损失的热量为 ![]() 。
。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户崔硕分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。