一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硫酸与水 B.生石灰与水
C.熟石灰与水 D.氯化钠与水
解析:浓硫酸溶于水虽然放热,但浓硫酸是液体,又具有强烈的腐蚀性,不适宜给食品加热;而相同质量的生石灰和熟石灰分别溶于水,前者放出的热量比后者多,氯化钠溶于水能量变化不明显。
答案:B
人造卫星常用的一种高能电池——银锌蓄电池,它在放电时的电极反应为:Zn+2OH--2e-===ZnO+H2O
Ag2O+H2O+2e-===2Ag+2OH-,据此判断氧化银是( )
A.负极,被氧化 B.正极,被还原
C.负极,被还原 D.正极,被氧化
解析:原电池就是把氧化还原反应拆分成氧化反应和还原反应两部分,分别在两个电极上发生,使电子经外电路移动,从而产生电流。
答案:B
下列反应属于放热反应的是( )
A.铁与盐酸反应
B.C与CO2共热
C.碳酸钙的分解
D.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
解析:Fe+2HCl===FeCl2+H2↑,放热反应;C+CO2![]() 2CO,吸热反应;CaCO3
2CO,吸热反应;CaCO3![]() CaO+CO2↑,吸热反应;Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O,吸热反应。
CaO+CO2↑,吸热反应;Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O,吸热反应。
答案:A
.假设某化学反应的反应过程如图所示,观察分析,符合图中变化的化学反应为( )
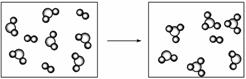
反应前 反应后
A.A2+3B2![]() 2AB3
2AB3
B.2AB2+B2![]() 2AB3
2AB3
C.2A2B+5B2===4AB3
D.2AB2+B2===2AB3
解析:由图可知反应物用AB2、B2表示,生成物用AB3表示,反应后反应物与生成物共存,说明反应不能进行到底,为可逆反应,结合反应前后原子守恒可知反应方程式为2AB2+B2![]() 2AB3。
2AB3。
答案:B
在恒温、恒容的容器中进行反应N2(g)+3H2(g)![]() 2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为( )
2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为( )
A.等于1.8 s B.等于1.2 s
C.大于1.8 s D.小于1.8 s
解析:氮气浓度降低0.1 mol·L-1-0.06 mol·L-1=0.04 mol·L-1需要2 s,若化学反应速率相等,则浓度降低0.06 mol·L-1-0.024 mol·L-1=0.036 mol·L-1需要时间为0.036 mol·L-1×2 s÷0.04 mol·L-1=1.8 s,但由于随着反应的进行,反应物的浓度不断减小,反应速率减小,故所用时间增长。
答案:C
本卷还有15题,登录并加入会员即可免费使用哦~

该作品由: 用户王娜分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。