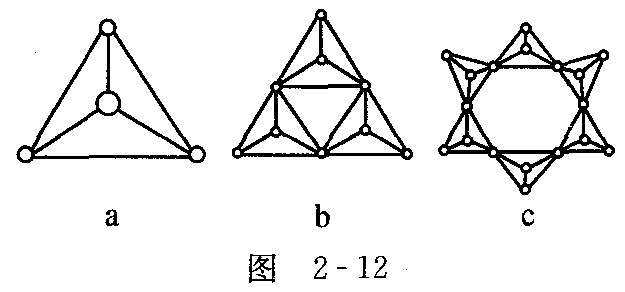
硅氧四面体可以用图2-12a表示,图中b、c是硅氧四面体结合成环状结构的两个例子.请回答下列问题:
(1)若在环状结构中硅的原子数为n,写出环状结构中硅酸根离子的通式_______.
(2)已知绿柱石是由环状硅氧四面体构成的硅酸盐.它是含有铍、铝两种元素的复盐,酸根中含有6个硅原子.写出绿柱石的化学式________,并在此基础上写成氧化物相结合的形式_______.
答案
思路分析
首先要注意观察图a,结合![]() 晶体中硅氧四面体的结构,不难想像到硅原子是位于硅氧四面体中心的;其次要分析图b、c所给出的两个环状结构,找出规律,并考虑Si在其中应呈+4价,便可写出通式;第三,当酸根中含有6个硅原子时,可按上述通式得出其负价总数为12,而铍、铝分别呈+2、+3价,据此便可确定该复盐中铍、铝的个数只能为3个、2个.至于改写成氧化物的形式只需注意各自的化合价即可.
晶体中硅氧四面体的结构,不难想像到硅原子是位于硅氧四面体中心的;其次要分析图b、c所给出的两个环状结构,找出规律,并考虑Si在其中应呈+4价,便可写出通式;第三,当酸根中含有6个硅原子时,可按上述通式得出其负价总数为12,而铍、铝分别呈+2、+3价,据此便可确定该复盐中铍、铝的个数只能为3个、2个.至于改写成氧化物的形式只需注意各自的化合价即可.
思维诊断
本题容易出现的错误有:
①不注意联系![]() 晶体中硅氧四面体的结构,错将硅氧四面体的组成理解为
晶体中硅氧四面体的结构,错将硅氧四面体的组成理解为![]() ,从而导致后续问题解答的连锁错误.
,从而导致后续问题解答的连锁错误.
②识图不够认真,缺乏空间想像,对氧原子的共用情况未做出准确判断.
③不注意Si在化合物中呈现+4价,因而错将其通式写成![]() .
.
④不会运用化合价规则判断该复盐中铍、铝的个数.在改写成氧化物的形式时未能注意按化合价规则分配氧原子.
[答案](1)![]() (2)
(2)![]()
![]() ,
,![]()


 表示,分子用化学式表示,离子用
表示,分子用化学式表示,离子用 表示。
表示。